1、选择题 短周期元素A、B、C原子序数依次递增,它们的原子的最外层电子数之和为10。A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数。下列叙述正确的是
A.原子半径B>C>A? B.氧化物的熔点B>A
C.A与C能形成离子化合物? D.氢化物的稳定性C>A
2、选择题 中学化学课本中有大量的数据材料,下面是某学生对数据的利用,其中不正确的是(? )
A.利用溶解度数据可判断煮沸Mg(HCO3)2溶液时,得到的产物是Mg(OH)2而不是MgCO3
B.利用密度数据可判断液态物质挥发性的大小
C.原子(或离子)半径数据可作为判断某些原子(或离子)的氧化性或还原性的依据
D.利用沸点数据可判断液态物质挥发性的大小
3、填空题 (14分)巳知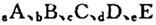 元索,
元索,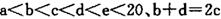 。A2为常温常压下密度最小的气体,B的单质有多种同素异形体,其中一种为质软灰黑色固体。C的最外层电子数是电子层数的2. 5倍。用E的单质制作的餐具不宜长期存放酸性、碱性或咸味食物。
。A2为常温常压下密度最小的气体,B的单质有多种同素异形体,其中一种为质软灰黑色固体。C的最外层电子数是电子层数的2. 5倍。用E的单质制作的餐具不宜长期存放酸性、碱性或咸味食物。
(1) B的原子结构示意图为_________;E在元素周期表中的位置________。
(2) 已知C2及其化合物有以下转化关系(部分物质已省略):

①将已收集满气体Y的试管管口倒扣在水面下,可以观察到的现象是________;其化学反应方程式为________; W的晶体类型为________;将E单质与Z的极稀溶液混合,还原产物只有W,则该反应的离子方程式为________________________。
②上述合成X的反应处于平衡状态时,气体X的浓度为C(X)(如图)。在恒温恒容条件下,t1时刻通人X将X的浓度变为2c(X)。请在下图画出平衡移动过程中X浓度的变化趋势图。
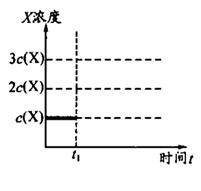
(3) 由其中三种元素形成的只含极性键、具有18电子的共价化合物为________ (写结构简式,至少2种)。
4、选择题 如图是元素周期表短周期元素的一部分。已知M最高价氧化物对应的水化物为常见的氧化性酸,下列说法正确的是:

A.M为氮元素
B.原子半径:Y>X
C.氢化物沸点:X>N
D.M、X、Y三种元素的最高价氧化物对应的水化物均为强酸
5、填空题 X、Y、Z、W是元素周期表中前30号元素,且原子序数依次增大。其相关信息如下表:
元素
| 相关信息
|
X
| X原子基态时最外层电子数是其内层电子总数的2倍
|
Y
| Y的基态原子最外层电子排布式为nsnnpn+2
|
Z
| Z元素的最高正价与负价代数和为6
|
W
| W基态原子未成对电子数是前30号元素中最多的
|
?
(1)W位于元素周期表第?周期第?族,其基态原子最外层有?个电子。
(2)X的第一电离能比Y的?(填“大”或“小”),1mol X22-中含有的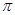 键数目为?。
键数目为?。
(3)X和Y的气态氢化物中,较稳定的是?(写化学式),Y的同族元素(包括Y)的最简单氢化物中沸点最低的是?。
(4)写出KZY3与HZ浓溶液反应制取Z2的化学方程式,并标出电子转移的方向和数目?。
(5)已知:X(s)+Y2(g)=XY2(g)? ΔH 1= -393.5 kJ?mol-1
XY(g) +1/2Y2(g)=XY2(g)? ΔH 2= -282.9 kJ?mol-1
则X(s)与Y2(g)反应生成XY(g)的热化学反应方程式为?。