1、选择题 依据氧化还原反应:2Ag+(aq) + Cu(s) ="=" Cu2+(aq) + 2Ag(s)设计的原电池如图所示。下列说法不正确的是

A.电极X的材料是铜
B.电解质溶液Y是硝酸银溶液;
C.银电极为电池的正极,发生的电极反应为:Ag+ + e- ="=" Ag
D.盐桥中的阳离子向硫酸铜溶液中运动
参考答案:D
本题解析:
答案:D
ABC均正确,在原电池内部,阳离子移向正极。阴离子移向负极,该电池银是正极,盐桥中的阳离子向硝酸银溶液运动。
本题难度:一般
2、选择题 下列说法正确的是(?)
A.4.0g碳化硅晶体中所含C―Si数为0.4NA
B.PCl3、BF3、HClO这些分子中每个原子都达到了8电子结构
C.电解精炼铜时,当阳极质量减少3.2 g时,电路中转移的电子数为0.1NA
D.若H+(aq) + OH-(aq)= H2O(l); kJ・mol-1,则含Ba(OH)2 1 mol溶液与1 mol稀H2SO4反应放出的热量为114.6 kJ
kJ・mol-1,则含Ba(OH)2 1 mol溶液与1 mol稀H2SO4反应放出的热量为114.6 kJ
参考答案:A
本题解析:略
本题难度:一般
3、选择题 如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是
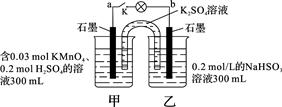
A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小
D.乙池中的氧化产物为SO42-
参考答案:C
本题解析:A.n(e-)=1.204×1022÷6.02×1023=0.02mol.则在乙烧杯中发生反应的NaHSO3的物质的量为0.01mol。产生的H+的物质的量为0.01mol。c(H+)=0.01mol÷0.1L=0.1mol/L。溶液中的H+主要是由NaHSO3反应产生。所以pH=1正确。B.在该原电池反应中,乙池的石墨电极为负极,甲池的石墨电极为正极。根据同种电荷相互排斥,异种电荷相互吸引的原则,电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a。正确。C.电池工作时,甲烧杯中MnO4-不断得到电子,变为Mn2+,消耗H+,溶液中的c(H+)不断减小,所以由水电离出的c(H+)逐渐增大。错误。D.在乙池中HSO3-不断被氧化,变为SO42-。因此该烧杯的氧化产物为SO42-。
本题难度:一般
4、简答题 在铜锌硫酸原电池中,锌为______极,______电子,电极发生的是______反应(填氧化或还原),电极反应式为______;铜为______极,______电子,电极发生的是______反应,电极反应式为______,铜片上观察到的现象为______.
参考答案:铜、锌、稀硫酸构成的原电池中,锌易失电子发生氧化反应而作负极,负极上电极反应式为 Zn-2e-=Zn2+;铜作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,铜电极上有氢气生成,所以看到的现象是铜片上有气泡产生,
故答案为:负;失;氧化;Zn-2e-=Zn2+;正;得;还原;2H++2e-=H2↑;有气泡产生.
本题解析:
本题难度:一般
5、选择题 糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
B.脱氧过程中铁作原电池正极,电极反应为:Fe-2e