1、实验题 为验证木炭可被浓硫酸氧化成二氧化碳,选用下图中仪器(含所盛物质)组装成套实验装置,试完成下列问题。?
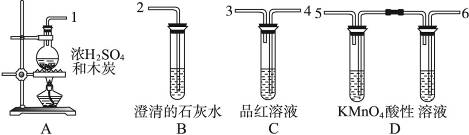
(1)在实验进行中,按气流方向从左到右的顺序,导管口的三处连接应该是____________接____________,____________接____________,____________接____________。?
(2)试管B、C中各有什么现象,才能表示已检出二氧化碳??
B中_________________________________,C中__________________________________。?
(3)试管D中能否用饱和NaHCO3溶液代替KMnO4酸性溶液?说明理由。
参考答案:(1)1 6 5 4 3 2
(2)澄清石灰水变浑浊 品红溶液不褪色
(3)不能。NaHCO3虽能除去SO2,但同时生成CO2,这样,使澄清石灰水变浑浊的CO2从何而来,不得而知。
本题解析:A中产生SO2和CO2:
C+2H2SO4 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
CO2能使澄清石灰水变浑浊,因此可用B装置检验是否有CO2生成;但SO2也能使澄清石灰水变浑浊,所以在将CO2通入B中前须除去SO2,除去SO2可用D?装置:?
2KMnO4+2H2O+5SO2====K2SO4+2MnSO4+2H2SO4
D装置是否将SO2气体除净了呢?可用C装置检验:若从D出来的气体不能使品红溶液褪色,则表明SO2已在D中被除净,这样B中澄清石灰水变浑浊,可确证有CO2生成。
本题难度:简单
2、选择题 将BaCl2溶液分别盛于两支试管中,第1支加入稀HNO3溶液,第2支加入烧碱溶液,然后再分别通入SO2气体,结果两试管均有白色沉淀产生。下列说法正确的是
A.证明SO2具有强氧化性和酸性
B.若第1支试管先通入Cl2,再通SO2气体,也有白色沉淀生成
C.若第2支试管先通入NH3,再通SO2,不会产生沉淀
D.若第1支试管中先加入稀HNO3溶液,再加入Na2SO3溶液,则无沉淀生成
参考答案:B
本题解析:首先明确SO2g与BaCl2不能反应,因为弱酸不能制取强酸,但:
第1试管:SO2被硝酸氧化为硫酸,遇BaCl2溶液生成硫酸钡沉淀
第2试管:SO2与碱生成亚硫酸盐,遇BaCl2而生成亚硫酸钡白色沉淀
分别体现了SO2的还原性及酸性氧化物的性质。
同样道理,其中的硝酸可用氯气代替,碱液可用氨水代替,SO2可用Na2SO3溶液代替。
本题难度:一般
3、选择题 17.2 g CaSO4・xH2O转变成2CaSO4・(x-1)H2O时,质量减少2.7 g,则x值是(?)
A.1
B.2
C.4
D.6
参考答案:B
本题解析:写出反应方程式,根据差量法计算。
2(CaSO4・xH2O)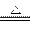 2CaSO4・(x-1)H2O+(x+1)H2O
2CaSO4・(x-1)H2O+(x+1)H2O
2(136+18x) g?18(x+1) g
17.2 g?2.7g
求得?x=2。
本题难度:简单
4、选择题 甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案:
方案①:铜与浓硫酸加热直接反应,即
方案②:由
请回答下列问题:
(1)“方案①”中铜和浓硫酸反应的化学方程式是______________________。
该反应体现了浓硫酸的__________性和____________性。
(2)这两种方案,你认为哪一种方案更合理?_______(答编号)。理由是____________。
参考答案:(7分)
27.(7分)
(1)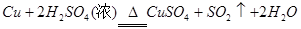 (2分)强氧化性?酸性
(2分)强氧化性?酸性
(2)②无污染产生,原料利用率高(2分)
本题解析:铜与浓硫酸反应中浓硫酸的性质,优化制硫酸的方案从环保和原子利用率的角度去考虑。
本题难度:一般
5、选择题 下列关于三氧化硫的叙述正确的是()
A.标准状况下三氧化硫是一种无色气体
B.三氧化硫与水反应放出大量的热
C.接触法制硫酸中常用水吸收三氧化硫
D.三氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水
参考答案:B
本题解析:此题主要考查三氧化硫的性质。物理性质:标准状况下为无色固体;化学性质:与水反应放出大量的热,生成硫酸,对应的盐为硫酸盐。
本题难度:简单