1、实验题 近几年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成的。
【实验目的】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】
(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),请完成该反应的离子方程式:
(?)SO2 +(?)MnO4― +(?)?=(?)??+(?)Mn2+ +(?)?
根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
【实验探究】甲同学:甲同学进行了如下图所示A、B两步实验:
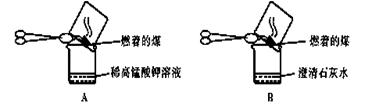
“实验现象”: A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
(2)乙同学认为甲的方案不合理,其理由是:?
【实验探究】丙同学:丙同学进行了如下图所示实验(部分装置在图中略去):
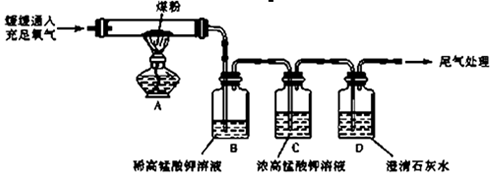
(3)上图C装置的作用是?
(4)证明煤中含有碳元素和硫元素的现象是: ?
(5)装置C中的高锰酸钾溶液也可以替换为?
A.足量I2的淀粉溶液? B.足量饱和NaHCO3溶液? C.足量Na2SO3溶液? D.足量溴水
参考答案:(1)( 5 )SO2 +( 2 )MnO4― +( 2 )H2O=( 5 )SO42-+( 2 )Mn2+ +( 4 )H+
(2)SO2也能使澄清石灰水变浑浊,不能证明煤中含有碳元素
(3)除去SO2并检验其是否除尽
(4)B中褪色, C中不褪色, D中变浑浊
(5)A D
本题解析:(1)在氧化还原反应中应该遵循质量守恒定律和电子守恒。由于该反应同时还是离子反应,因此还应该符合电荷守恒。该反应方程式为5SO2 +2MnO4― +2 H2O=5+ SO42-+2Mn2+ + 4H+。(2)A中稀高锰酸钾溶液褪色证明含有SO2;B中澄清石灰水变浑浊,则可能是SO2使澄清石灰水变浑浊的,也可能是SO2与CO2共同作用的结果。因此不能证明煤中含有碳元素。(3)在装置A中使煤充分燃烧,通过B稀酸性高锰酸钾溶液来检验SO2;通过C浓酸性高锰酸钾溶液来除去SO2,以确保完全除尽。然后在通过D澄清石灰水来检验CO2气体。若澄清的石灰水变浑浊,则证明含有CO2,否则就不含有CO2。(4)证明煤中含有硫元素的现象是B中褪色,证明含有碳元素的现象是C中不褪色, D中变浑浊。(5)高锰酸钾溶液有强氧化性,可以把SO2氧化为硫酸。若用其它物质来代替,只要物质有强氧化性,可以与SO2发生氧化还原反应即可。A.I2+SO2+2H2O=H2SO4+2HI。溶液的紫色褪去。正确。B.NaHCO3+SO2= NaHSO3+CO2.虽然能除去SO2,但是能产生CO2,会影响CO2的检验。错误。C.Na2SO3+SO2+2H2O=2NaHSO3,由于该溶液呈碱性,也能吸收CO2,所以会影响CO2的检验。错误。D.足量溴水,发生反应:Br2+SO2+2H2O=H2SO4+2HBr。但是与CO2不能发生反应,所以可以除去SO2来检验CO2。正确。因此选项为AD。
本题难度:一般
2、填空题 储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化汽化法提纯。其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3、H2O七种物质。
(1)请用上述物质填空,并配平化学方程式:
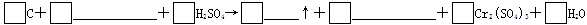
(2)上述反应中氧化剂是(填化学式)_______________,被氧化的元素是(填元素符号)_____________。
(3)H2SO4在上述反应中表现出来的性质是(填选项编号)____________________。
A.氧化性 ?B.酸性? C.氧化性和酸性?D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为________升。
参考答案:(1)3? 2K2Cr2O7? 8? 3CO2? 2K2SO4? 2? 8? (共2分,其中配平1分,化学式1分)
(2)K2Cr2O7?C? (各2分)
(3)B? (1分)
(4)4.48? (2分)
本题解析:(1)由C→CO2、K2Cr2O7→Cr2(SO4)3可知,碳元素的化合价从0价升高到+4价,失去4个电子。Cr元素的化合价从+6价降低到+3价,得到3个电子,所以根据电子得失守恒可知还原剂与氧化剂的物质的量之比是3:2。根据原子守恒可知,反应中还有硫酸钾生成,则反应的化学方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。
(2)根据(1)可知氧化剂为K2Cr2O7,还原产物为Cr2(SO4)3,还原剂为C,氧化产物为CO2,被氧化的元素是C。
(3)H2SO4在反应中各元素的化合价没有发生变化,但反应中有硫酸盐生成,所以硫酸只表现酸性,答案选B。
(4)设产生的气体的体积为V,根据反应式计算:
3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O转移电子
33.6L? 12mol
V?0.8mol
解得V=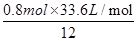 =4.48L
=4.48L
本题难度:一般
3、填空题 我国了“神舟”系列载人飞船的成功发射,标志着“炎黄子孙千年飞天梦想实现了”
(1)火箭升空时,由于与大气层的剧烈摩擦,产生高温。为了防止火箭温度过高,在火箭表面涂上一种特殊的涂料,该涂料的性质最可能的是___________________
A.在高温下不融化
B.在高温下可分解气化
C.在常温下就分解气化
D.该涂料不可能发生分解
(2)火箭升空需要高能的燃料,经常是用N2O4和N2H4作为燃料,其反应的方程式是:
N2O4 + N2H4 → N2 + H2O 。
①请配平该反应方程式:____N2O4 + ____N2H4 → ____N2 + ____H2O
②该反应中被氧化的原子与被还原的原子物质的量之比是____________。
③这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是________________________。
(3)为了向宇航员提供氧气,飞船上有专门的供氧装置。现有供氧剂过氧化钠与超氧化钾(KO2)。
①写出它们与二氧化碳反应的化学方程式(超氧化钾与二氧化碳的反应产物与过氧化钠类似):
______________________;_________________________。
②你选择的供氧剂是:____________________,原因是:____________________________。
参考答案:(1)B
(2)①1、2、3、4;②2∶1;③产物无污染
(3)① 2Na2O2+2CO2==2Na2CO3+O2;4KO2+2CO2==2K2CO3+3O2?
②KO2;单位质量产生氧气多
本题解析:
本题难度:一般
4、计算题 3.16 g KMnO4与50mL 12 mol・L-1过量浓盐酸完全反应(假设浓盐酸无挥发),化学方程式如下:2KMnO4+16HCl=2KCl+2MnCl 2+ 5Cl2↑+8H2O,?通过计算回答:
(1)未被氧化的HCl的物质的量是?;
(2)产生的Cl2在标准状况下的体积为多少升?
(3)在反应后的溶液中加足量的AgNO3溶液可生成多少克沉淀?
参考答案:0.06mol 1.12L? 71.75g
本题解析:KMnO4的物质的量=3.16/158=0.02,设需要HCl的物质的量是Xmol,生成Cl2的物质的量是Ymol,MnCl 2的物质的量为Zmol。
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
2? 16? 5
0.02? X? Y
得:X=0.16? Y=0.05?
根据氧化反应的概念可知,元素的化合价升高被氧化,Cl元素的化合价一部分升高,一部分不变,所以HCl是部分被氧化.从化学方程式可以看出,16个Cl原子中有10个原子的化合价升为0价,因此未被氧化HCl占总的HCl的6/16,因此被氧化的HCl的物质的量=0.16×6/16=0.06mol。故Cl2在标准状况下的体积=0.×22.4=1.12L。氯离子的物质的量为0.05L×12 mol・L-1-0.05mol×2=0.5mol,故氯化银的质量为0.5mol×(108g/mol+35.5g/mol)=71.75g。
本题难度:简单
5、实验题 (7分)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米管伴有大量的杂质――碳纳米颗粒。这种碳纳米颗粒可用氧化法提纯。其原理可表示为:
□C+ □K2Cr2O7+ □H2SO4=□CO2+ □Cr2(SO4)3+ □K2SO4+□H2O
(1)请配平上述化学方程式, 将有关的化学计量数依次填在下列横线上
??、?、?、?、?、?、?
(2)上述反应中的氧化剂是(填化学式,下同)?,还原剂是?。
(3)H2SO4在上述反应中表现出的性质是(填选项序号)?。
A.氧化性
B.氧化性和酸性
C.酸性
D.还原性和酸性