1、选择题 用铂电极电解一定浓度的下列物质的水溶液,在电解后的电解液中加适量水,能使溶液浓度恢复到电解前浓度的是(?)
A.NaCl
B.Na2CO3
C.CuSO4
D.K2S
参考答案:B
本题解析:加适量水能使溶液恢复到电解前的浓度,则电解的实质是电解水,故选项B符合。
本题难度:一般
2、选择题 进行电解水的实验时,为增强水的导电性,需向水中加入一定量的电解质。下列物质中可以加入的是(?)
A.AgNO3
B.NaCl
C.H2SO4
D.NaOH
参考答案:CD
本题解析:电解的是水,只是为增强水的导电性,所加入的物质本身不参与反应。而AgNO3和NaCl加入后,溶液中所增加的Ag+>H+与Cl->OH-,故,H2SO4和NaOH符合题意。
本题难度:简单
3、填空题 如下图是一个乙醇燃料电池工作示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
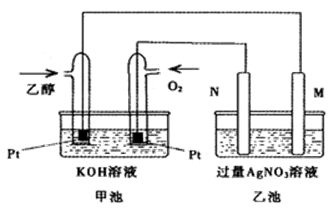
(1)M电极材料是 , N的电极反应式为 ,加入乙醇的铂电极的电极反应式为 。
(2)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出约为30kJ热量,表示乙醇燃烧热的热化学方程式为 。
(3)若M、N均为石墨电极,将乙池改为电解500mL含KNO3和Cu(NO3)2的混合液一段时间后,在两极上均生成11.2L(标准状况)气体。则M极产生的气体是H2,原混合液中Cu2+的物质的量浓度是 mol/L。
参考答案:(共8分)
(1)铁 (1分) 4OH―-4e―=2H2O+O2↑ (1分)C2H5OH-12e+16OH―=2CO32―+11H2O (2分)
(2)C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=-1380kJ/mol (2分)
(3)1 mol/L (2分)
本题解析:(1)甲池是燃料电池,乙池是电解池,通入氧气的一极是正极,则N极是阳极,则M极是阴极,M、N两个电极的质量都不减少,则铁作阴极,所以M极的材料是铁;N极发生氧化反应,根据离子的放电顺序,则在N极放电的书写氢氧根离子,失去电子生成氧气,电极反应式为4OH―-4e―=2H2O+O2↑;加入乙醇的一极是原电池的负极,发生氧化反应,结合电解质溶液,生成碳酸根离子和水,电极反应式为C2H5OH-12e+16OH―=2CO32―+11H2O;
(2)1mol乙醇的质量是46g,所以1mol乙醇完全燃烧生成CO2和液态H2O时放出46×30kJ=1380kJ的热量,所以乙醇燃烧的热化学方程式为C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=-1380kJ/mol ;
(3)若M、N均为石墨电极,将乙池改为电解500mL含KNO3和Cu(NO3)2的混合液,当M极放出氢气时,说明铜离子放电完全,N极产生氧气,根据4OH―-4e―=2H2O+O2↑,可知生成标准状况下11.2L氧气,失去电子的物质的量是11.2L/22.4L/mol×4=2mol,生成11.2L氢气时得到电子的物质的量是11.2L/22.4L/mol×2=1mol,则铜离子共得到1mol电子,根据Cu2++2e-==Cu,可知铜离子的物质的量是1/2mol,所以原混合液中Cu2+的物质的量浓度是1/2mol/0.5L=1.0mol/L。
考点:考查电化学反应原理的应用,氧化还原反应的计算
本题难度:一般
4、计算题 铁是地壳中含量第二的金属元素,其单质、合金及化合物在生产生活中的应用广泛。
(
参考答案:
本题解析:
本题难度:困难
5、填空题 已知:Ksp(AgCl)=1.8×10―10,Ksp(AgI)=1.5×10―16 ,Ksp(Ag2CrO4)=2.0×10―12,Ag2CrO4为砖红色沉淀。
(1) AgCl、AgI、 Ag2CrO4三种饱和溶液中,Ag+浓度由大到小顺序是 。现将等体积2.0×10―4 mol・L-1的AgNO3溶液和一定浓度的Na2CrO4溶液混合,若要产生Ag2CrO4沉淀,则Na2CrO4溶液至少浓度为 mol・L-1。
(2) 在室温下,向0.02mol・L-1的Na2CrO4溶液中滴加0.01mol・L-1稀硫酸,溶液由黄色转变为橙红色的Na2Cr2O7,该平衡转化的离子方程式为 。Na2Cr2O7可用来鉴别NaCl和NaNO2,鉴别时发生的离子方程式为 。
(3) 工业酸性废水中含Cr2O72-离子会造成铬污染,排放前先将Cr2O72-还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气。结果溶液的pH值不断升高,溶液由酸性转变为碱性。在以上处理过程中,写出其阳极电极反应式: ,Cr2O72-转化为毒性较低的Cr3+的离子方程式为: 。
(4) 用AgNO3溶液滴定含Cl-的溶液,可测定溶液中的c(Cl-)。可滴入几滴 溶液为指示剂,滴定的终点现象为 。
参考答案:(14分)
(1)Ag2CrO4>AgCl>AgI 4.0×10―4 (各2分)
(2)2 CrO42-+2 H+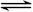 Cr2O72-+ H2O Cr2O72-+3NO2-+8H+="3" NO3-+2 Cr3++4H2O (各2分)
Cr2O72-+ H2O Cr2O72-+3NO2-+8H+="3" NO3-+2 Cr3++4H2O (各2分)
(3)Fe-2e-=Fe2+ Cr2O72-+6 Fe2++14H+="6" Fe3++2 Cr3++7 H2O(各2分)
(4) Na2Cr2O7 (或K2Cr2O7或含Cr2O72-) 加入最后一滴AgNO3溶液出现砖红色沉淀(各1分)
本题解析:
(1)根据Ksp进行计算,可以得到Ag+浓度大小关系,混合后c(Ag+)=1×10-4mol/L,Ksp=c2(Ag+)c(CrO42-),从而求出c(CrO42-)=2.0×10-4mol/L,故Na2CrO4浓度为4.0×10- 4mol/L。
(2)黄色转化为橙色,是铬酸根转化为重铬酸根,用重铬酸钠来鉴别,是应为NaNO2具有较强的还原性,可以与重铬酸根发生氧化还原反应,根据氧化还原反应基本原理可以写出化学方程式。
(3)阳极发生氧化反应,因为使用铁做电解,为活性电极,优先放电,故Fe-2e-=Fe2+;二价铁具有还原性,可将重铬酸根还原,生成三价铬,然后转化为氢氧化铬沉淀。
(4)根据上面数据可以看出,氯离子先与铬酸根与银离子产生沉淀,故可以用重铬酸根或铬酸根,氯离子沉淀完全,生成砖红色沉淀。
考点:考查沉淀溶解平衡、电解以及滴定等知识。
本题难度:困难