1、选择题 用惰性电极电解CuSO4溶液一段时间后,停止电解,向所得溶液中加入0.1 mol Cu(OH)2,溶液浓度恢复至电解前。关于该电解过程的说法不正确的是
A.生成Cu的物质的量是0.1 mol
B.转移电子的物质的量是0.2 mol
C.随着电解的进行溶液的pH减小
D.阳极反应式是4OH--4e-=2H2O+O2↑
2、选择题 下列说法正确的是( )
①可用电解饱和NaCl溶液的方法制取金属钠
②铝热反应一定是氧化还原反应
③以煤、石油和天然气为原料,通过化学反应可获得许多性能优异的合成高分子材料
④含硫化石燃料的大量燃烧是形成酸雨的主要原因.
A.①②③
B.②③④
C.②③
D.①②③④
3、填空题 选考题【化学一一选修化学与技术】(15分)以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol・L-1计算)。
金属离子
| 开始沉淀的pH
| 沉淀完全的pH
|
Fe3+
| 1. 1
| 3. 2
|
Zn2+
| 5. 2
| 6. 4
|
Fe2+
| 5. 8
| 8. 8
|
(1)加入H2O2溶液发生反应的离子方程式为 。
(2)流程图中,为了降低溶液的酸度,试剂X不可以是 (选填序号:
a.ZnO;b.Zn(OH)2 ;c.Zn2(OH)2CO3;d.ZnSO4;pH应调整到 ;
(3)氯化锌能催化乳酸(2-羟基丙酸)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为 ;
Ⅱ、制取金属锌采用碱溶解ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq),然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ;阴极的电极反应为 ;
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 。
4、选择题 如下图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是
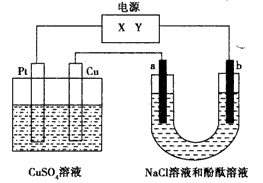
? [? ]
A.X极是电源负极,Y极是电源正极
B.a极的电极反应是2Cl--2e-==Cl2↑
C.电解过程中CuSO4溶液的pH逐渐增大
D.Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体
5、选择题 下列有关工业生产的叙述正确的是
A.合成氨生产过程中将NH3液化分离,会降低反应速率,可提高N2、H2的转化率
B.从海水中提镁过程中,电解熔融MgO可制备Mg
C.电解精炼铜时,同一时间内阳极溶解固体的质量比阴极析出固体的质量小
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室