|
|
|
高中化学知识点总结《原电池原理》考点巩固(2019年最新版)(三)
2019-06-28 20:49:35
【 大 中 小】
|
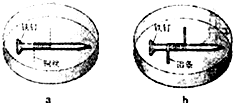
1、选择题 如题图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )
A.a中铁钉附近呈现红色
B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应
D.b中铝条附近有气泡产生
| 
2、选择题 分析下图所示的四个原电池装置,其中结论正确的是
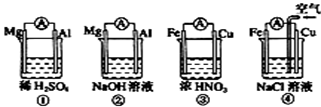
A.①②中Mg作为负极,③④中Fe作为负极
B.②中Mg作为正极,电极反应式为6H2O + 6e-
|
3、填空题 (6分)(1)X、Y、Z三种金属,X、Y组成原电池,X是负极;把Y放在Z的硝酸盐溶液中,Y表面有Z析出。其活泼顺序是_________________;
(2)由氢气和氧气反应生成1mol水蒸气放热241.8 kJ,写出该反应的热化学方程式:___________________________ _______。
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是 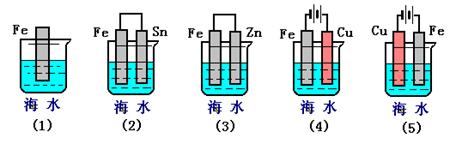
4、选择题 下列有关电化学知识的描述正确的是? ( )
A.CaO+H2O=Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能
B.某原电池反应为Cu+2AgNO3=Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液
C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极
D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池
5、选择题 将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如下图所示。最先观察到变为红色的区域为( )
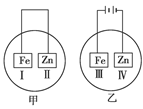
A.Ⅰ和Ⅲ
B.Ⅰ和Ⅳ
C.Ⅱ和Ⅲ
D.Ⅱ和Ⅳ


