| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ���ܽᡶԭ���ԭ�������㹮�̣�2019�����°棩(��)
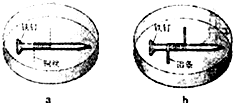 �ο��𰸣�A��a�й��ɵ�����ͭԭ��أ�����Ϊ������Fe-2e-=Fe2+������������Ӧ��û�к�ɫ���֣���A���� ��������� �����Ѷȣ�һ�� 2��ѡ���� ������ͼ��ʾ���ĸ�ԭ���װ�ã����н�����ȷ���� |
�ο��𰸣�
���������
�����Ѷȣ�һ��
3������� ��6�֣���1��X��Y��Z���ֽ�����X��Y���ԭ��أ�X�Ǹ�������Y����Z����������Һ�У�Y������Z�����������˳����_________________��
��2����������������Ӧ����1molˮ��������241.8 kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��___________________________ _______��
(3)���и������������FeƬ��ʴ�ɿ쵽����˳���� 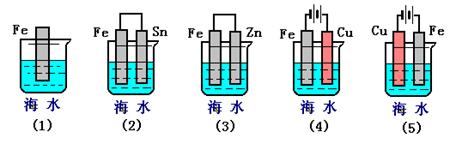
�ο��𰸣���1��X>Y>Z
��2��2H2(g)+O2(g)=2H2O(g) ��H=��483.6 kJ��mol��1
(3) �ɢƢŢǢ�
�����������1����ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ��X��Y���ԭ��أ�X�Ǹ��������X�Ľ�����ǿ��Y��Y����Z����������Һ�У�Y������Z��������Y�Ľ�����ǿ��Z�����Խ�����ǿ��˳����X>Y>Z��
��2��������������Ӧ����1molˮ��������241.8 kJ�����Ը÷�Ӧ���Ȼ�ѧ����ʽ�ǣ�2H2(g)+O2(g)=2H2O(g) ��H=��483.6 kJ��mol��1��
��3������װ��ͼ��֪����1��װ�������Ļ�ѧ��ʴ����2������3����ԭ��أ����У�2�������Ǹ������ٸ�ʴ����3������������������������4������5���ǵ��أ����У�4������������������������5��������������ʧȥ���ӣ��ӿ츯ʴ��������Ƭ��ʴ�ɿ쵽����˳���ǢɢƢŢǢȡ�
�����Ѷȣ�һ��
4��ѡ���� �����йص绯ѧ֪ʶ��������ȷ����? (����)
A��CaO��H2O=Ca(OH)2�����Էų��������ȣ��ʿɰѸ÷�Ӧ��Ƴ�ԭ��أ������еĻ�ѧ��ת��Ϊ����
B��ijԭ��ط�ӦΪCu��2AgNO3=Cu(NO3)2��2Ag��װ���е������п�����װ�к�������KCl������Һ
C����Ϊ���Ļ�����ǿ��ͭ�����Խ�����ͭ�õ������Ӻ����Ũ�����У��������ԭ��أ���������������ͭ������
D��������˵���κ����Է����е�������ԭ��Ӧ������Ƴ�ԭ���
�ο��𰸣�D
���������A�CaO��H2O=Ca(OH)2����������ԭ��Ӧ��������Ƴ�ԭ��أ�B��ᷢ����Ӧ��KCl��AgNO3=AgCl����KNO3�����ɵ�AgCl��ʹ���ŵĵ����Լ��������Բ���ʹ��KCl��Һ���ɻ���KNO3��Һ��B�����C�����������Ũ����ᷢ���ۻ���������������Ĥ���ʸ���ϲ��ܹ���ԭ��ء�����C�����D����ȷ��
�����Ѷȣ�һ��
5��ѡ���� ����Ƭ��пƬ����ʢ��NaCl��Һ(���е��з�̪)�ı������У�����ͼ��ʾ�����ȹ۲쵽��Ϊ��ɫ������Ϊ(����)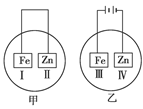
A����͢�
B����͢�
C����͢�
D����͢�
�ο��𰸣�B
�����������ͼʾ��ԭ��أ�п��������пʧ�����γ�п���ӣ������Ǣ��������ϣ�O2+2H2O+4e-=4OH-�����Ԣ�죻��ͼʾ�ǵ��أ�������������ʧ���������������ӣ�п���������������ϣ�2H++2e-=H2�����ƻ���пƬ����ˮ�ĵ���ƽ�⣬ʹ��OH-Ũ���������Ԣ���Ҳ��죮��ѡB��
���������⿼����ԭ��غ͵��صĹ���ԭ����Ӧ�ã���Ҫ�ǵ�ⷴӦ�����ӱ仯��
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ�ؿ�֪ʶ�㡶�����йص�.. | |
| �����Ŀ |