1、选择题 下列说法不正确的是
[? ]
A.向纯水中加入盐酸使水的电离平衡逆向移动,水的离子积减小?
B.反应NH3(g)+HCl(g)==NH4Cl(s)?△H<0,低于一定温度自发,高于一定温度非自发
C.铅蓄电池在放电过程中,负极质量减少,正极质量增加
D.用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3?
参考答案:AC
本题解析:
本题难度:一般
2、选择题 常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图。下列判断错误的是
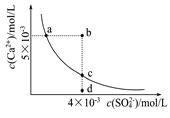
A.a、c两点均可以表示常温下CaS04溶于水所形成的饱和溶液
B.a点对应的Ksp不等于c点对应的Ksp
C.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L
D.向d点溶液中加入适量CaCl2固体可以变到c点
参考答案:B
本题解析:
考查Ksp。Ksp是一个常数,只跟温度有关,温度不变溶度积常数不变。a、c恰好为平衡点,d为不饱和溶液;b为过饱和溶液,将有晶体析出;
B.a点对应的Ksp等于c点对应的Ksp
本题难度:简单
3、填空题 向含有AgI的饱和溶液中分别加入下列物质,请就溶液中碘离子浓度的变化做出回答。(1)加入固体AgNO3:________________________________________
(2)若改加更多的AgI固体:________________________________________
(3)若改加AgBr固体:________________________________________
参考答案:(1)减小? (2)不变? (3)减小
本题解析:根据同离子效应对平衡的影响,可以判断加入固体AgNO3和AgBr会使的溶解平衡向左移动,碘离子浓度变小;而在饱和溶液中再加入AgI固体对平衡无影响。
本题难度:一般
4、填空题 (14分)滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)酸碱中和滴定 用标准盐酸滴定未知浓度的NaOH溶液。
①酸式滴定管、碱式滴定管、温度计、量筒、玻璃棒、烧杯。若要进行中和滴定实验,还缺少的玻璃仪器是 。
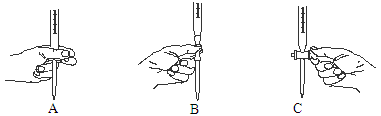
②上述滴定过程中操作滴定管的图示,正确的是 。
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得NaOH 溶液浓度 (填“偏大”、“偏小”或“无影响”)。
(2)氧化还原滴定 用标准高锰酸钾溶液滴定未知浓度的草酸(H2C2O4)溶液。
①课外小组里有位同学设计了下列两种滴定方式(夹持部分略去),引起了同学们的讨论,最后取得识,你认为合理的是 (填字母序号)。

②判断滴定终点的依据是 。
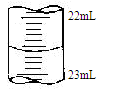
③某次滴定时记录滴定前滴定管内液面读数为0.50mL,滴定后液面如图,则此时消耗标准溶液的体积为 。
(3)沉淀滴定 滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。
参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选的指示剂是 (填选项字母)。
难溶物
| AgCl
| AgBr
| AgCN
| Ag2CrO4
| AgSCN
|
颜色
| 白
| 浅黄
| 白
| 砖红
| 白
|
KSP
| 1.77×10-10
| 5.35×10-13
| 1.21×10-16
| 1.12×10-12
| 1.0×10-12
|
A、NaCl B、NaBr C、NaCN D、Na2CrO4
参考答案:(1)①锥形瓶 ② A ③无影响(2)①b [来源:Z§xx§k.Com]②溶液恰好由无色变浅紫红色,且半分钟内不 褪 色 ③22.10mL(3)D
本题解析:(1)①进行酸碱中和滴定实验时,待测液要装在锥形瓶中,所以还缺少锥形瓶。②在进行滴定操作是时,要用左手控制酸式滴定管的活塞,所以A对,C错,挤压碱式滴定管的玻璃球时要往外挤压,B错。③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,对NaOH物质的量没有影响,所以再继续滴定至终点,盐酸的用量不变,故对所测得NaOH 溶液浓度没有影响。(2)①酸性高锰酸钾有强氧化性,要用酸式滴定管装,所以b对。②草酸溶液是无色的,高锰酸钾溶液是紫色的,所以滴定终点的现象为:当滴最后一滴高锰酸钾溶液时,溶液恰好由无色变浅紫红色,且半分钟内不褪色。③滴定后滴定管的读数为22.60mL,此时消耗标准溶液的体积为22.60mL-0.5 mL=22.10mL。(3)用AgNO3滴定NaSCN溶液生成的AgSCN是白色沉淀,为了现象明显,指示剂不能再是白色的,排除AgCl 和AgCN,在根据沉淀滴定的原理:滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。选D。
考点:酸碱中和滴定、氧化还原滴定和沉淀滴定的误差分析、指示剂的选择、滴定终点的判定等。
本题难度:困难
5、填空题 (16分)氨气是一种重要的化工产品及工业原料。
I.某温度下,合成氨反应的平衡常数K=3.0×103(mol/L)-1,
(1)写出其对应的化学方程式____________________________________________________ 。
(2)某温度下,如果在体积恒定为10L的密闭容器中充入:0.1molN2、0.1molH2和2molNH3则反应_______(填“正向进行”或“逆向进行”或“达到平衡”)。
(3)该温度下,在体积恒定为10L的四个密闭容器中分别充入下列物质,反应达到平衡后,N2的转化率最大的是___________________。
a.10molN2、30molH2和20molNH3 b.10molN2和30molH2
c.20molN2和60molH2 d.10molN2和28molH2
II.氨气极易溶于水,氨水是氨气溶于水而形成的溶液,回答下列问题:
(4)在氨水溶液中加水稀释的过程,NH3・H2O的电离程度___________(填“增大”“减小”或“不变”),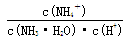 ___________(同上)。
___________(同上)。
(5)室温下,a mol/L的(NH4)2SO4水溶液的pH=5,原因是溶液中存在平衡________________________(用离子方程式表示)。并计算该平衡的平衡常数表达式为________________________(用含代数a的较为精确的数学表达式表示,不必化简,不做近似运算)。
(6)室温下,向浓度均为0.1mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为_________________________________________。
(已知:室温时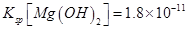 mol3
mol3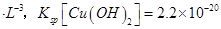 mol3.L-3).
mol3.L-3).
参考答案:Ⅰ. (1)1/2 N2 + 3/2 H2 NH3(2分) (2)正向进行(2分) (3)c(2分)
NH3(2分) (2)正向进行(2分) (3)c(2分)
Ⅱ.(4)增大(1分) 不变 (2分)
(5)NH4++H2O NH3?H2O+H+(2分) 10-5(10-5-10-9)/2a+10-9-10-5 mol・L-1(2分)
NH3?H2O+H+(2分) 10-5(10-5-10-9)/2a+10-9-10-5 mol・L-1(2分)
(6)Cu(OH)2(1分) Cu2++2NH3・H2O=Cu(OH)2 ↓+2NH4+(2分)
本题解析:(1)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,则根据平衡常数可知反应的化学方程式为1/2 N2 + 3/2 H2 NH3。
NH3。
(2)在体积恒定为10L的密闭容器中充入:0.1molN2、0.1molH2和2molNH3则产生浓度熵为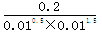 =2000<3000,所以反应向正反应方向进行。
=2000<3000,所以反应向正反应方向进行。
(3)a与b相比,a中含有大量的氨气,因此b中氨气的转化率大于a中。b与d相比,b中氢气浓度大,大转化率高;由于正方应是体积减小的可逆反应,所以增大压强平衡向正反应方向进行,c与b相比,相当于是在b的基础上增大压强,氮气转化率增大,答案选c。
(4)稀释促进氨水的电离,电离程度增大。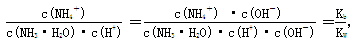 ,因此比值不变。
,因此比值不变。
(5)铵根水解溶液显酸性,方程式为NH4++H2O NH3?H2O+H+。室温下,在a mol?L-1的(NH4)2SO4水溶液中pH=5,溶液中c(H+)=10-5mol/L,故溶液中c(OH-)=10-9mol/L,根据电荷守恒有:c(NH4+)+c(H+)=c(OH-)+2c(SO42-),即c(NH4+)+10-5mol/L=10-9mol/L+2amol/L,则c(NH4+)=(2a+10-9-10-5)mol/L,根据物料守恒计算溶液中c(NH3?H2O)=2amol/L-(2a+10-9-10-5)mol/L=(10-5-10-9)mol/L,故NH4++H2O
NH3?H2O+H+。室温下,在a mol?L-1的(NH4)2SO4水溶液中pH=5,溶液中c(H+)=10-5mol/L,故溶液中c(OH-)=10-9mol/L,根据电荷守恒有:c(NH4+)+c(H+)=c(OH-)+2c(SO42-),即c(NH4+)+10-5mol/L=10-9mol/L+2amol/L,则c(NH4+)=(2a+10-9-10-5)mol/L,根据物料守恒计算溶液中c(NH3?H2O)=2amol/L-(2a+10-9-10-5)mol/L=(10-5-10-9)mol/L,故NH4++H2O NH3?H2O+H+的平衡常数的表达式为
NH3?H2O+H+的平衡常数的表达式为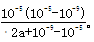 。
。
(6)溶度积常数越小的物质越先沉淀,氢氧化铜的溶度积小于氢氧化镁的溶度积,所以氢氧化铜先沉淀,铜离子和氨水反应生成氢氧化铜沉淀和铵根离子,离子方程式为Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+。
考点:考查平衡常数计算与应用、外界条件对电离平衡的影响、盐类水解以及溶度积常数应用等
本题难度:困难