1、实验题 合肥市某校化学兴趣小组为探究铁与浓硫酸反应,设计了如图所示装置进行实验。
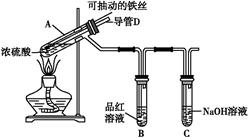
(1)实验过程中,观察到B中的实验现象是? 。
一段时间后,观察到从C中有少量的气泡冒出,此气泡的成分是 ?。
(2)用“可抽动的铁丝”代替“直接投入铁片”的优点是? ;
反应结束后,不需要打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是? 。
(3)反应一段时间后,他们对A中溶液的金属阳离子进行了探究。
①提出假设:
假设1:溶液中只存在Fe2+;
假设2: ?;?
假设3:溶液中存在Fe2+和Fe3+。
②请你设计实验验证上述假设1,写出实验操作步骤、实验现象及结论。限选试剂:酸性KMnO4溶液、NaOH溶液、淀粉KI溶液、KSCN溶液。
?
2、填空题 (1)铜是人类最早使用的金属之一,以下是冶炼铜的一个反应:
Cu2S+2Cu2O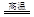 6Cu+SO2
6Cu+SO2
该反应中被氧化的元素是?,若反应中转移1mol电子,得到Cu?mol。?
(2)下列两种方法均可以制备CuSO4。
方法一:2Cu+O2 2CuO,CuO+H2SO4=CuSO4+H2O
2CuO,CuO+H2SO4=CuSO4+H2O
方法二:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
①假如某工厂欲生产CuSO4,请选择一种方法,并说明理由:?
?。
②有同学认为,生成等量的硫酸铜两种方法消耗的能量相同,因为反应都是铜转变为CuSO4,你认为上述说法?(填“正确”或“不正确”),原因是?
?。
3、填空题 A、B、C、D为四种中学化学中常见的单质。常温时A为淡黄色固体,B也是固体且B可被磁化;C和D是双原子分子的气体,C呈黄绿色。E、F、G、H、I为五种化合物,E难溶于水,F为气体,且极易溶于水得无色酸性溶液;H溶于水后得黄色或棕黄色溶液。它们之间有如下反应的转化关系:
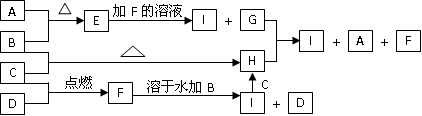
(1)四种物质的化学式:B________,C_______,E________,F_______;
(2)物质I溶液的颜色呈_______色;
(3)用实验方法鉴别H和I可用__________试剂,现象是_________________;
 (4)写出G+H? I+A+F的离子方程式_______________________________。
(4)写出G+H? I+A+F的离子方程式_______________________________。
4、填空题 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)FeCl3溶液与金属铜发生反应的离子方程式是?。
(2)检验溶液中Fe3+存在的操作步骤和现象是?。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得氯化铁溶液,准备采用下列步骤:
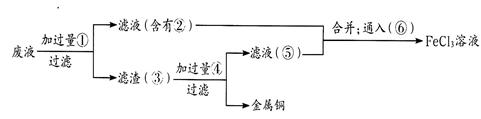
上述实验中加入或生成的有关物质的化学式为②??④____________
通入⑥得到FeCl3溶液的离子反应方程式为________________。
5、选择题 下列物质在常温下可用铁质容器盛放的是
A.亚硫酸
B.浓硫酸
C.浓盐酸
D.胆矾溶液