1������� ij�¶��£�һ�����Ļ���������ܱ������з������·�Ӧ��mA(��)+nB(��)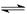 pC(��)��ƽ������������С��ԭ����
pC(��)��ƽ������������С��ԭ���� �����ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ����1.9������ѹ�������б����¶Ȳ��䣬��Ӧ����ʽ������ϵ����ϵ�ǣ�?��
�����ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ����1.9������ѹ�������б����¶Ȳ��䣬��Ӧ����ʽ������ϵ����ϵ�ǣ�?��
�ο��𰸣�m+n��p��
���������
�����������m��n��p
�����⡿�¶�һ��������������С��ԭ���Ķ���֮һ���������ʵ�Ũ�ȶ�������Ӧ�ı仯���൱�ڸ���ϵ��ѹ��Ӧ��ѹǿ�����ı䣬����ƽ���ƶ��������ۡ�������ij���ʵ�Ũ�ȱ仯ʱ������Ҫ��ƽ���ƶ����棨��ѧ�仯�����ǡ���Ҫ��ѹǿ��������仯����������Ũ�ȱ仯���������أ����濼�ǡ����ӵ������������Ȼ�ó�����Ľ��ۡ��磺���Ӽ�ѹ����ƽ���ƶ����ǣ�C��Ũ��Ϊԭ����1.9����һ����ƽ��������Ӧ�����ƶ��Ľ������Ӧ������������ʵ�����������������������ʵ�������m+n=p��
���⿼�ǵ������С��ԭ���Ķ���֮һ��һ˲�䣬�������ʵ�Ũ�Ƚ�����ԭ���Ķ�����C��Ũ��ҲӦΪԭ���Ķ�������Ŀ�����йشﵽ��ƽ��ʱC��Ũ��Ϊԭ����1.9������ζ��ƽ�������淴Ӧ�����ƶ�����ˣ�����Ϊ��m+n��p��
�����Ѷȣ���
2��ѡ���� ��һ�������£������ܱ������н��еķ�Ӧ��
A(g)+B(g) C(g)+D(g)
C(g)+D(g)
�����������˵����һ��Ӧ�Ѿ��ﵽƽ��״̬���ǣ�?��
A.A��B��C��D��Ũ�����? B.A��B��C��D���ܱ������й���
C.A��B��C��D��Ũ�Ȳ��ٱ仯? D.A���ĵ�������C���ĵ��������
�ο��𰸣�C
�����������ѧƽ��ı����������������淴Ӧ������ȣ����־��Ǹ����ʵ�Ũ�Ȳ��ٱ仯��
�����Ѷȣ�һ��
3������� (6��)���ܱ������н������·�Ӧ��mA(g)��nB(g)  pC(g)����Ӧ��5 min�ﵽƽ�⣬��ô�ʱA��Ũ�ȼ�С��a mol��L��1����C��Ũ��������2/3a mol��L��1����֪ƽ����Ӧ����v(C)��2v(B)��
pC(g)����Ӧ��5 min�ﵽƽ�⣬��ô�ʱA��Ũ�ȼ�С��a mol��L��1����C��Ũ��������2/3a mol��L��1����֪ƽ����Ӧ����v(C)��2v(B)��
(1)д��������ѧ����ʽ�и����ʵļ�������m��________��n��________��p��________
(2)ѹǿһ��ʱ��C�İٷֺ���(C%)���¶ȡ�ʱ��(T��ʾ�¶ȣ�t��ʾʱ��)�Ĺ�ϵ��ͼ��ʾ���ɴ˿�֪���÷�ӦΪ��?(����ȡ����ȡ�)��Ӧ��

(3)�÷�Ӧ��ƽ�ⳣ����ʾʽΪ�����������������������¶ȣ�Kֵ��������(���������С�����䡱)��
�ο��𰸣���6�֣���(1)3��1��2��ÿ��1�֣��� (2)���ȣ�1�֣�
(3)K��c2(C)/c3(A).c(B)?��2�֣���С��2�֣�
�����������1��ƽ����Ӧ����v(C)��2v(B)������B��Ũ�ȼ�����1/3amol/L�����ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪��m�Un�Up��3�U1�U2������m��3��n��1��p��2��
��2������ͼ���֪��T1���ȴﵽƽ��״̬�������¶���T1����T2���¶ȸߣ�C�İٷֺ����ͣ�˵�������¶�ƽ�����淴Ӧ������У���������Ӧ�Ƿ��ȷ�Ӧ��
��3��ƽ�ⳣ������һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ������ƽ�ⳣ���ı���ʽ��K��c2(C)/c3(A).c(B)�������¶�ƽ�����淴Ӧ������У�������ƽ�ⳣ���Ǽ�С�ġ�
�����Ѷȣ�һ��
4������� (10��)����ЧӦ����Դ��ȱ ���������ν��ʹ����е�CO2���������Կ������������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)��3H2(g)?
���������ν��ʹ����е�CO2���������Կ������������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)��3H2(g)?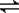 ?CH3OH(g)��H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯��
?CH3OH(g)��H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯��
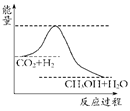
(1)���ڸ÷�Ӧ������˵���У���ȷ����________��
A����H>0����S>0
B����H>0����S<0
C����H<0����S<0
D����H<0����S>0
(2)�÷�Ӧƽ�ⳣ��K�ı���ʽΪ________________________________��
(3)�¶Ƚ��ͣ�ƽ�ⳣ��K________(����������䡱��С��)��
(4)Ϊ̽����Ӧԭ�����ֽ�������ʵ�飺�����Ϊ1 L���ܱ������У�����1 mol CO2��3 mol ?H2�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ���ӷ�Ӧ��ʼ��ƽ�⣬������Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(H2)________mol��L��1��min��1��
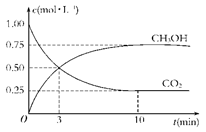
(5)���д�ʩ����ʹn(CH3OH)/n(CO2)�������________��
A�������¶�
B���������
C����H2O(g)����ϵ�з���
D���ٳ���1 mol CO2��3 mol H2
E������He(g)��ʹ��ϵ��ѹǿ����
�ο��𰸣�(1)C�� (2)��(3)����? (4)0.225 ��(5)CD
�����������
�����Ѷȣ�һ��
5��ѡ���� ��ijһ�ݻ�Ϊ2L���ܱ������ڣ�����0��2mol��CO�� 0��2mol�� H2O��g�����ڴ������ڵ������º����·������·�Ӧ��CO��g����H2O��g��?����CO2��g����H2��g������H��a kJ/mol��a��0������Ӧ�ﵽƽ����c��CO����c��CO2����3��2������˵����ȷ���ǣ�?��
A������ϵѹǿ����ʱ��Ӧһ���ﵽƽ��
B����Ӧ�ų�������Ϊ 0��2a kJ
C���������¶ȣ�v�������ӿ죬 v���棩������ƽ�������ƶ�
D������ͬ�������ټ���0��2mol��CO��0��2mol�� H2O��g�������´�ƽ��ʱ��c��CO����c��CO2����3��2
�ο��𰸣�D
�����������
�����Ѷȣ���