|
|
|
高考化学试题《热化学方程式》高频试题特训(2019年最新版)(七)
2019-06-28 22:45:23
【 大 中 小】
|
1、选择题 下列说法不正确的是
A.若2H2(g)+O2(g)=2H2O(g) ΔH=
|
2、填空题 A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下:
元素
| 相关信息
| A
| A元素原子核外只有三个能级,且每个能级上含有相等的电子数
| B
| 是空气中含量最丰富的元素
| C
| 短周期中,单质C的金属性最强
| D
| 基态原子第三能层上有7种运动状态不同的电子
| E
| 一种核素的质量数为63,中子数为34
|
请用对应的元素符号回答下列问题:
(1)A与氢可形成一种的分子式为A2H4化合物,该分子中存在σ键与π键数目比为 。
(2)H―A、H―B两种共价键中,键能较大的是 ;H―A、H―D两种共价键中,键的极性较强的是
(3)E位于周期表中的位置是 ,单质E与B的最高价氧化物的水化物的稀溶液反应的离子方程式为 。
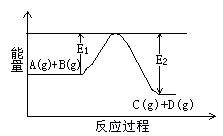
(4)根据下列能量变化示意图,请写出BO和AO2反应的热化学方程式 。

(5)C的最高价氧化物对应的水化物为M,M中含有的化学键类型为 。将一定量的D2通入一定浓度M的水溶液中,两者恰好完全反应时,生成物中有三种含D元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如上图所示。请写出t2时刻总反应方程式
3、填空题 (10分)回答下列问题:
(1)反应A(g)+B(g) C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0(填“>”、“<”、 C(g)+D(g)过程中的能量变化如右图所示,判断该反应△H 0(填“>”、“<”、
或“无法确定”)。
(2)在Al2O3、Ni催化下气态甲酸发生下列反应:
甲酸(g)=" CO" (g)+ H2O (g) △H1=" +34.0" kJ/mol
甲酸(g)= CO2 (g)+ H2(g) △H2=" ―7.0" kJ/mol
则甲酸的分子式为 ,在该条件下,气态CO2和气态H2反应生成气态CO和气态H2O的热化学方程式为 。
(3)如图所示,水槽中试管内有一枚铁钉,放置数天观察:

I若试管内液面上升,则正极反应: 。
II若试管内液面下降,则发生 腐蚀。
III若溶液甲为水,溶液乙为海水,则铁钉在 (填“甲”或“乙”)溶液中腐蚀的速度快。
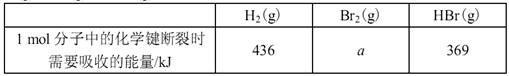
4、选择题 已知H-H键能436kJ/mol;Cl-Cl键能243kJ/mol;H-Cl键能431kJ/mol,则下列热化学方程式正确的是( )
A.H2(g)+Cl2(g)=2HCl(g)△H=-183?kJ/mol
B. H2(g)+Cl2(g)=HCl(g)△H=-124kJ/mol
C.2HCl(g)=H2(g)+Cl2(g)△H=-248?kJ/mol
D.HCl(g)=H2(g)+Cl2(g)△H=-91.5?kJ/mol
5、填空题 (1)稀强酸、稀强碱反应生成1mol液态水时放出57.3 kJ的热量。
① 实验室中可用稀盐酸和氢氧化钡稀溶液反应来测定中和热。请写出能表示该反应中和热的热化学方程式___________________________;
② 分别取100 mL 0.50 mol/L盐酸与100 mL 0.55 mol/L NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。假设盐酸和氢氧化钠溶液的密度都是1g/cm3,中和后生成溶液的比热容
c = 4.18 J/(g・℃)。实验时,测得反应前盐酸与NaOH溶液的平均温度为21.5℃,反应后混合溶液的温度为24.9℃。则实验测得的中和热△H=_______(保留1位小数);
③ 如果用含1 mol CH3COOH的稀醋酸与足量稀氢氧化钠溶液反应,反应放出的热量____________57.3 kJ(填“大于”、“小于”或“等于”);理由是_____________________________。
(2)在催化剂的作用下CH4还原NO可以得到三种产物(该条件下均为气体),利用此反应能消除环境污染物NO。理论上每消耗标况下22.4 L NO就能放出290kJ的热量。写出该反应的热化学方程式
___________________________。
|
