|
|
|
高中化学必备知识点《水的电离平衡》高频考点巩固(2019年模拟版)(一)
2019-06-28 22:56:44
【 大 中 小】
|
1、选择题 关于常温下0.1 mol・L-1醋酸钠溶液,下列说法正确的是
A.水电离出来的c(OH-)=1.0×10-13 mol・L-1
B.该溶液的pH<13
C.溶液中离子浓度关系:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.加入等浓度等体积的盐酸,溶液中:c(CH3COOH)+ c(CH3COO-)= c(Cl-)+ c(Na+)
|
2、填空题 工业上利用含有一定浓度的I2和CuSO4溶液的工业废水制备饲料添加剂Ca(IO3)2,其生产流程如下:

已知:Ca(IO3)2微溶于水,溶于硝酸;Ksp(CuI)=1.1×10-12, Ksp(Cu2S)=2.5×10-48;
氧化性: HNO3>IO3―>H2O2
(1)“还原”过程中主要反应的化学方程式为:2Na2S2O3+I2 = + 2NaI。
(2)在还原过程还伴随有CuI生成,写出加入Na2S的离子反应方程式 。
(3)在氧化过程中先加入H2O2再加入浓硝酸,而不直接加入浓硝酸的目的是 。
(4)加入的石灰乳在溶液中反应而得到Ca(IO3)2,则要调节pH至 (填“酸性” 或“中性”或“碱性”),原因是 。
(5)Ca(IO3)2也可用电化学氧化法制取:先充分电解KI溶液,然后在电解后的溶液中加入CaCl2,最后过滤得到Ca(IO3)2。写出电解时阳极发生的电极反应方程式 ,用该方法制取Ca(IO3)2,每1kg碘化钾理论上可生产纯度为97.8%Ca(IO3)2的质量为 ____kg(计算结果保留3位有效数字)。
3、填空题 写出下列物质的电离方程式:
HNO3______
Ba(OH)2______
KClO3______.
4、选择题 25°C时,pH=7的(NH4)2SO4与NH3・H2O的混合溶液中,c(NH )与c(SO )与c(SO )之比是 ( ) )之比是 ( )
A.等于2∶1
B.大于 2∶1
C.小于2∶1
D.无法判断
|
5、填空题 (12分)回答下列问题:
(1) 常温下,pH=5的盐酸和pH=9的氢氧化钠溶液按体积比9∶11混合,混合后溶液的pH为
(2)NH4Cl溶液显酸性,试用离子方程式 表示这一反应_____________________。
表示这一反应_____________________。
(3)已知水的电离方程式可写为2H2O 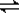
 表示这一反应_____________________。
表示这一反应_____________________。