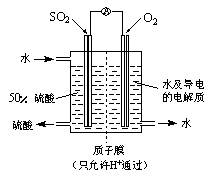
1��ѡ���� ��������ʵ�Ľ��ʹ������(? )
A��������ˮ����Ȫʵ�飬˵��������������ˮ
B�������£���ͭ����Ũ�����������Ա仯��˵��ͭ�����Ũ�����жۻ�
C��Ũ��������Ի�ɫ��˵��Ũ������в��ȶ���
D�����м���Ũ�������ְ�ɫ������˵��ŨH2SO4������ˮ��
2��ѡ���� ��FeCl3��BaCl2�Ļ����Һ��ͨ��SO2����Һ��ɫ���ػ�ɫ���dz��ɫ��ͬʱ�а�ɫ��������������˵����ȷ����(�� ��)
A����ʵ�����FeCl3�л�ԭ��
B����ɫ����ΪBaSO3
C����ʵ�����SO2��Ư����
D����Ӧ����Һ������ǿ
3������� ��һ�������������ƾ����ֱ����������ʣ�Ϊ�˲ⶨ��Ʒ�����ʵ�����������������ʵ����̣���Ҫ����д�ո�
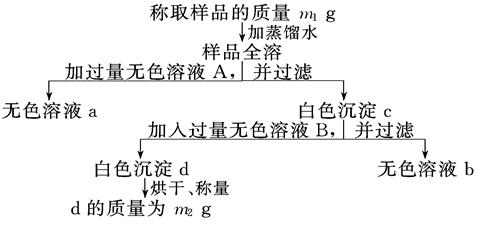
��1��������Һ�м������ɫ��ҺA��____________���ѧʽ����A���������ԭ����
________________________________________________________________________��
��2����ɫ����c�к���____________________���ѧʽ����
��3����ɫ��ҺBͨ����_____________�����Լ����ƣ����������c��Ӧ�����ӷ���ʽΪ
________________________________________________________________________��
��4��ͨ�����ϲⶨ�ɵõ���Ʒ�����ʵ����������ļ���ʽΪ_______________________��
4��ѡ���� ���Ȼ�����Һ��ͨ��SO2���ް�ɫ���������������Ȼ�����Һ��װ����ֻ�Թ��У�һ֧�����ᣬ��һ֧��NaOH��Һ��Ȼ���ٷֱ�ͨ��������SO2�������֧�Թ��ж��а�ɫ�������ɡ��ɴ˵ó����н�����ȷ����
A������NaOH����ҺpH���ߣ�c(SO32��)����
B���Ȼ���������
C����֧�Թ��еİ�ɫ��������BaSO4
D��SO2����������ˮ��Һ������
5������� �������й�SO2��Cl2������ʵ�顣
��1��ijС�������ͼ��ʾ��װ��ͼ��ͼ�мгֺͼ���װ����ȥ�����ֱ��о�SO2��Cl2�����ʡ�
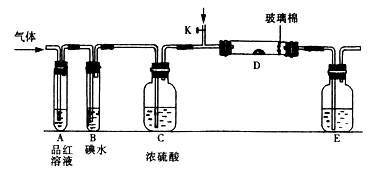
��������˷ֱ�ͨ��SO2��Cl2��װ��A�й۲쵽�������Ƿ���ͬ��?(���ͬ������ͬ��)����D��ʢͭ�ۣ�ͨ��������Cl2��D�е�������___________����װ��D��װ��������������(����)��ͨ��SO2ʱ����Kͨ������O2�Ļ�ѧ��Ӧ����ʽΪ?��
��SO2ͨ��B�У���ˮ��ɫ����÷�Ӧ�����ӷ���ʽΪ?��
��E��ʢ��______________��Һ��
��2��ijͬѧ��������SO2ͨ��һ֧װ���Ȼ�����Һ���Թܣ�δ���������ɣ�������Թ��м�������(����ĸ)?������Կ�����ɫ����������
A����ˮ
B��ϡ����
C��ϡ����
D���Ȼ�����Һ