1、填空题 如图每一方框中的字母代表一种反应物或生成物。产物J是含金属元素A的白色胶状沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白。
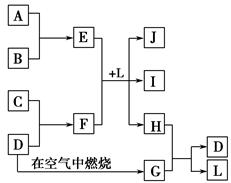
(1)框图中所列物质中属于非电解质的物质的化学式是?。
(2)用电子式表示出H的形成过程?。
(3)将E的水溶液蒸干并灼烧得到的固体物质的化学式为?。
(4)F的水溶液中各离子浓度由大到小的顺序为?。
(5)F的水溶液显碱性的原因:?(用离子方程式表示)。
(6)E与F在L中反应的离子方程式为?。
(7)H和G之间反应的化学方程式为?。
2、选择题 能证明SO2具有漂白性的是
A.酸性KMnO4溶液中通入SO2气体后溶液褪色
B.滴入酚酞的NaOH溶液中通入SO2气体红色消失
C.品红溶液中通入SO2气体红色消失
D.溴水中通入SO2气体后溶液褪色
3、实验题 为了探究SO2与Na2O2的反应是否类似于CO2,甲同学设计了如图实验装置。
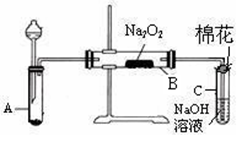
回答下列问题:
(1)制取SO2的合适试剂是 ?。
a.80%的H2SO4(aq)?b.10%的H2SO4(aq)?
c.Na2SO3(s)?d.Na2SO3(aq)?
(1)装置C中NaOH(aq)的作用是?。
(1)移开棉花,将带火星的木条放在C试管口,未见木条复燃。甲同学因此认为SO2与Na2O2的反应不同于CO2。请按甲同学的观点写出反应的化学方程式?。
(1)检验反应后B装置中生成物的方法是?。
(1)乙同学认为无论反应原理如何,最终都有O2产生。乙同学的理由是?。按照乙同学的观点,该装置还需作如下改进:?。(简要阐述,并指明必需的装置名称与试剂。)
4、选择题 向100 mL含等物质的量的HBr和H2SO3的溶液里通入0.01 mol Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3)。则原溶液中HBr的物质的量浓度为(? )
A.0.007 5 mol・L-1
B.0.008 mol・L-1
C.0.075 mol・L-1
D.0.08 mol・L-1
5、选择题 往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时产生白色沉淀。下列有关说法中不正确的是(?)
A.白色沉淀为BaSO4
B.反应后溶液的pH减小
C.此实验表明SO2有漂白性
D.此实验中Fe3+表现出氧化性