1、选择题 将a mol FeCl3和b mol FeS混合物加入到某浓度的氢硫酸中,充分反应后,氢硫酸的浓度没有改变(不考虑溶液体积的变化),则a、b的关系是(?)
A.a>2b
B.a="b"
C.a≤ 2b
D.a ≥b
参考答案:C
本题解析:略
本题难度:简单
2、实验题 将过量的SO2分别通入下列溶液:①氢硫酸②溴水③品红溶液④澄清石灰水⑤酸性高锰酸钾⑥氯化钙溶液,根据要求填空。
(1)无明显现象的是?;
(2 )溶液颜色褪去的是?;
)溶液颜色褪去的是?;
(3)SO2作氧化剂的是?;
(4)SO2作还原剂的是?;
(5)先生成沉淀然后沉淀溶解的是?;
(6)有沉淀生成且沉淀不溶解的是?。
参考答案:( 1)⑥?(2)②③⑤?(3)①?(4)②⑤?(5)④?(6)①
1)⑥?(2)②③⑤?(3)①?(4)②⑤?(5)④?(6)①
本题解析:略
本题难度:简单
3、实验题 硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(该反应△H>0)。某研究小组在实验室用硫化碱法制备Na2S2O3・5H2O流程如下。

(1)吸硫装置如图所示。

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ??,表明SO2吸收效率低的实验现象是B中溶液 ??。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是 ?、??。(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。(室温时CaCO3饱和溶液的pH=10.2)
限选试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管
序号
| 实验操作
| 预期现象
| 结论
|
①
| 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,___________________。
| _______________
| 样品含NaCl
|
②
| 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,___________________。
| _______________
| 样品含NaOH
|
?
(3)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:准确称取a g KIO3(化学式量:214)固体配成溶液,加入过量KI固体和H2SO4溶液,滴加指示剂,用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=_________mol・L-1。(只列出算式,不作运算)
已知:Cr2O72-+6I-+14H+= 2Cr3++3I2+7H2O? 2S2O32-+I2=S4O62-+2I-
(4)某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的Na2S2O3浓度可能?(填“无影响”、“偏低”或“偏高”),原因是?。
参考答案:(1)①品红、溴水或KMnO4溶液;溶液颜色很快褪色或指出相应试剂的正确颜色(红色、黄色等)很快褪色也可得分。?(2分,每个1分)
②增大SO2的接触面积、控制SO2的流速、适当升高温度(答其中二条即可)(4分,每个2分)
(2)(8分,每个2分)
序号
实验操作
预期现象
①
滴加足量稀硝酸,再滴加少量AgNO3溶液,振荡。
有白色沉淀生成
②
加入过量CaCl2溶液,搅拌,静置,用pH计测定上层清液pH
有白色沉淀生成,上层清液pH大于10.2
?
(3)6000a/214V 或3000a/107V? (其它正确答案也给分)?(2分)
(4)偏高;4I―+4H++O2=2I2+2H2O
本题解析:(1)①由于SO2具有还原性、漂白性,因此若 装置B的作用是检验装置A中SO2的吸收效率,则B中试剂可以是品红、溴水或KMnO4溶液,表明SO2吸收效率低的实验现象是B中溶液溶液颜色很快褪色。
②要使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是增大SO2的接触面积、控制SO2的流速、适当升高温度等。
(2)氯离子的检验可以利用硝酸酸化的硝酸银溶液;由于饱和碳酸钙溶液的pH=10.2,所以可以先进入氯化钙溶液,然后测量溶液的pH值进行对比即可,因此答案为:
序号
实验操作
预期现象
①
滴加足量稀硝酸,再滴加少量AgNO3溶液,振荡。
有白色沉淀生成
②
加入过量CaCl2溶液,搅拌,静置,用pH计测定上层清液pH
有白色沉淀生成,上层清液pH大于10.2
?
(3)ag硝酸钾的物质的量是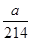 mol,则根据反应式IO3-+5I-+6H+=3I2+3H2O、2S2O32-+I2=S4O62-+2I-可知:IO3-~~~~~6S2O32-
mol,则根据反应式IO3-+5I-+6H+=3I2+3H2O、2S2O32-+I2=S4O62-+2I-可知:IO3-~~~~~6S2O32-
1mol? 6mol
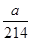 mol?
mol?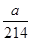 mol×6
mol×6
所以c(Na2S2O3)=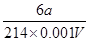 mol/L=
mol/L=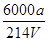 mol/L
mol/L
(4)由于碘离子易被氧化:4I―+4H++O2=2I2+2H2O,因此如果第三步滴速太慢,则导致消耗的硫代硫酸钠溶液的体积增加,从而导致其浓度偏高。
本题难度:困难
4、填空题 假设116号元素存在,完成下列问题:?
(1)116号元素在元素周期表中的位置是___________________________________。?
(2)下列关于116号元素的说法中正确的是_________________。?
A.无氧酸钠盐的化学式为Na2R的形式?
B.最高价氧化物可能是碱性氧化物?
C.原子的近似相对原子质量必定为332?
参考答案:(1)第七周期、ⅥA族 (2)B
本题解析:已知元素的原子序数判断元素在周期表中的位置,方法之一是参照ⅠA族和0族元素原子序数法。元素周期表第七周期的ⅠA族元素原子序数为87,0族元素原子序数为118,87<116<118。故116号元素在周期表的第七周期、倒数第三个族――ⅥA族。
周期表第ⅥA族第五周期的元素碲虽然为非金属元素,但有一定的金属性,如单质碲为银白色、能导电。根据周期表同主族内元素性质变化的规律判断可知,116号元素是金属元素,且其金属性较强或很强。金属元素的最高价氧化物可能是碱性氧化物,但它不存在无氧酸,自然就没有Na2R这种形式的盐。
原子的近似相对原子质量就是原子的质量数。元素原子序数是116,该元素中可能有同位素,或者说该元素可能包括两种或更多种不同的核素。在现有条件下,不能确定该元素中任何一种核素原子核内的中子数,也就不能确定原子的近似相对原子质量。
本题难度:简单
5、实验题 已知盐酸加到品红溶液中,使品红溶液的红色加深。试推测:
 (1)向品红溶液中通过量SO2的过程中的现象为__________;加热后的现象为_______。
(1)向品红溶液中通过量SO2的过程中的现象为__________;加热后的现象为_______。
 (2)向品红溶液中通入过量Cl2的过程中,观察到的现象为____________。
(2)向品红溶液中通入过量Cl2的过程中,观察到的现象为____________。
 (3)向品红溶液中通入物质的量比为1∶1且足量的SO2和Cl2后现象为___________。
(3)向品红溶液中通入物质的量比为1∶1且足量的SO2和Cl2后现象为___________。
参考答案: (1)溶液颜色先变深后又逐渐褪去?逐渐恢复原来的红色。
(1)溶液颜色先变深后又逐渐褪去?逐渐恢复原来的红色。
 (2)溶液的颜色先变深后又逐渐褪去,不再恢复红色(或仍为无色)。
(2)溶液的颜色先变深后又逐渐褪去,不再恢复红色(或仍为无色)。
 (3)溶液的红色比原来加深。
(3)溶液的红色比原来加深。

本题解析:当向品红溶液中通入过量的SO2时,发生如下反应:SO2+H2O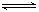 H2SO3,生成的酸能使品红溶液红色加深,因SO2过量,SO2与品红溶液结合成不稳定的无色物质而褪色,加热,无色物质分解又逐渐恢复到原来的红色。当向品红溶液中通入Cl2,因Cl2+H2O
H2SO3,生成的酸能使品红溶液红色加深,因SO2过量,SO2与品红溶液结合成不稳定的无色物质而褪色,加热,无色物质分解又逐渐恢复到原来的红色。当向品红溶液中通入Cl2,因Cl2+H2O

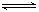 HClO+HCl同样生成了酸,品红溶液红色加深,因Cl2过量,Cl2氧化有色物质而褪色,加热后不再恢复红色,当向品红溶液中通入1∶1的SO2和Cl2时,两者发生以下反应:Cl2+SO2+2H2O
HClO+HCl同样生成了酸,品红溶液红色加深,因Cl2过量,Cl2氧化有色物质而褪色,加热后不再恢复红色,当向品红溶液中通入1∶1的SO2和Cl2时,两者发生以下反应:Cl2+SO2+2H2O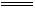 2HCl+H2SO4,因生成了酸,使品红溶液颜色加深。
2HCl+H2SO4,因生成了酸,使品红溶液颜色加深。
本题难度:一般