1、选择题 下列反应可用H++OH-=H2O表示的是
A.HCl+NH3・H2O
B.HCl+Ba(OH)2
C.H2SO4+Fe(OH)3
D.CH3COOH+NaOH
参考答案:B
本题解析:A中NH3・H2O为弱碱,C中Fe(OH)3不溶,D中CH3COOH为弱酸.
本题难度:简单
2、选择题 某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)
A.Na+
B.CO32-、NH4+
C.CH3COO-
D.CH3COO-、Na+
参考答案:C
本题解析:试题分析:某溶液中含大量NH4+、Na+、HCO3-、CO32-、CH3COO-离子,其中加入足量的Na2O2固体后,首先Na2O2先和水反应生成氢氧化钠和氧气,钠离子变大,HCO3-与氢氧根反应生成CO32-,所以HCO3-变小、CO32-变大,故选C。
考点:离子反应,过氧化钠的性质。
点评:离子反应,离子共存的变形形式,抓住题眼,找到突破口。
本题难度:困难
3、选择题 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的体积的关系可表示为?
[? ]
A.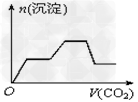
B.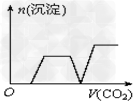
C.
D.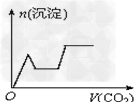
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列离子组在一定条件下能大量共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是?(?)?
选项
| 离子组
| 加入试剂
| 加入试剂后发生反应的离子方程式
|
A
| Fe2+、NO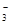 、K+ 、K+
| 稀硫酸
| 3Fe2++NO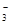 +4H+=3Fe3++NO↑+2H2O +4H+=3Fe3++NO↑+2H2O
|
B
| Fe3+、I-、ClO-
| 氢氧化钠溶液
| Fe3++3OH-=Fe(OH)3↓
|
C
| Ba2+、HCO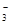 、Cl- 、Cl-
| 氢氧化钠溶液
| HCO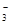 + OH-=CO + OH-=CO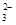 +H2O +H2O
|
D
| Al3+、Cl-、NO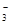
| 过量氢氧化钠溶液
| Al3++3 OH-=Al(OH)3↓
参考答案:A
本题解析:A、Fe2+、NO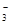 、K+可以大量共存,加入稀硫酸后,溶液中相当于存在稀硝酸,与Fe2+发生氧化还原反应生成Fe3+、NO,离子方程式符合书写原则,正确;B、Fe3+、ClO-与I-因发生氧化还原反应不能大量共存,错误;C、Ba2+、HCO 、K+可以大量共存,加入稀硫酸后,溶液中相当于存在稀硝酸,与Fe2+发生氧化还原反应生成Fe3+、NO,离子方程式符合书写原则,正确;B、Fe3+、ClO-与I-因发生氧化还原反应不能大量共存,错误;C、Ba2+、HCO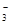 、Cl-可以大量共存,加入氢氧化钠溶液后,OH-与Ba2+、HCO 、Cl-可以大量共存,加入氢氧化钠溶液后,OH-与Ba2+、HCO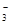 反应生成碳酸钡沉淀,离子方程式书写错误;D、Al3+、Cl-、NO 反应生成碳酸钡沉淀,离子方程式书写错误;D、Al3+、Cl-、NO 可以大量共存,加入过量氢氧化钠溶液,Al3+与3OH-反应生成AlO2-而不是Al(OH)3沉淀,错误,答案选A。 可以大量共存,加入过量氢氧化钠溶液,Al3+与3OH-反应生成AlO2-而不是Al(OH)3沉淀,错误,答案选A。
本题难度:一般
5、选择题 下列各组离子以适当比例混合,可以形成无色透明碱性溶液的是
A.Na+、 Ba2+、OH-、SO42-
B.Ag+、NH4+、OH-、NO3-
C.Mg2+、Na+、AlO2-、OH-
D.MnO4-、Al3+、SO42-、Cl-
参考答案:B
本题解析:
本题难度:困难
|