1������� ��10�֣�Mn��Fe��Ϊ�������ڹ���Ԫ�أ���Ԫ�صIJ��ֵ����ܣ�I�����������±���
Ԫ��
| 25Mn
| 26Fe
|
������/kJ��mol��1
| I1
| 717
| 759
|
I2
| 1509
| 1561
|
I3
| 3248
| 2957
|
?�ش��������⣺
��1��MnԪ����Χ���Ӳ�ĵ����Ų�ʽΪ?���Ƚ���Ԫ�ص�I2��I3��֪����̬Mn2+��ʧȥһ�����ӱ���̬Fe2+��ʧȥһ�������ѡ��Դˣ���Ľ�����?��
��2��Feԭ�ӻ�������Χ�н϶���������Ŀչ��������һЩ���ӻ������γ���������Feԭ�ӻ������γ������ķ��ӻ�����Ӧ�߱���������?��
��3�����Ȼ���������Ϊ���壬�۵�282�棬�е�315�棬��300��������������������ˮ��Ҳ���������ѡ���ͪ���л��ܼ����ݴ��ж����Ȼ�������Ϊ ?���塣
��4���������ľ����ڲ�ͬ�¶��������ֶѻ���ʽ�������ֱ�����ͼ��ʾ������������������������������ʵ�ʺ��е�Feԭ�Ӹ���֮��Ϊ?��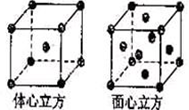
�ο��𰸣���1��3d54s2?��Mn2+ 3d�ܼ������Ų�Ϊ����״̬�����ȶ��ṹ��
��������2���йµ��Ӷԡ�����3�����ӡ�����4��1��2
�����������1�����ݹ���ԭ����д��MnԪ����Χ���Ӳ�ĵ����Ų�ʽ���̵�ԭ��������25��������Χ���Ӳ�ĵ����Ų�ʽΪ3d54s2 ����Mn2+��3d�ܼ������Ų�Ϊ����״̬�����ȶ��ṹ�����������ӵ�3d�ܼ�����6�����ӣ������ȶ��ṹ��
��2��Ҫд����λ�������������ṩ�µ��ӶԵ����塣
��3���Ȼ�����300��������������˵���þ���Ӧ���Ƿ��Ӿ��塣
��4�������ֶѻ���ʽ�к��е���ԭ�ӷֱ�Ϊ��1��8��1/8=2��6��1/2��8��1/8=4�����Ժ��е�Feԭ�Ӹ���֮����1�U2��
�����Ѷȣ�һ��
2��ѡ���� ����Ԫ�� �ķ����������ش�Ƽ��ɹ�֮һ����������֧���ˡ��ȶ����������С�ħ������Ŀ�����Ӻ����ӵ�ԭ�Ӻ˵Ļ�ѧԪ���ر��ȶ����ļ�˵��ԭ��
�ķ����������ش�Ƽ��ɹ�֮һ����������֧���ˡ��ȶ����������С�ħ������Ŀ�����Ӻ����ӵ�ԭ�Ӻ˵Ļ�ѧԪ���ر��ȶ����ļ�˵��ԭ�� ������������������֮��Ϊ
������������������֮��Ϊ
A��0
B��118
C��57
D��175
�ο��𰸣�C
����������ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ���������ݴ˿�֪�ú��ص���������118����������293.����Ϊ����������������������������������������������Ըú��ص�����������������֮��Ϊ293��118��118��57����ѡC��
�����������Ǹ߿��еij������ͣ��������¿Ƽ����·���Ϊ���壬�ص㿼��ѧ����ԭ������Լ������֮��������ϵ����Ϥ�˽�̶ȣ������ڵ���ѧ����ѧϰ��Ȥ������ѧ��ѧϰ��ѧ�Ļ����ԡ�
�����Ѷȣ���
3��ѡ���� ����˵����ȷ���ǣ�?��
A���ǽ���Ԫ�س��ֵ�����ϼ۲�������Ԫ��ԭ�ӵ�����������
B���ǽ���Ԫ�س��ֵ���ͻ��ϼۣ������ֵ���ڸ�Ԫ��ԭ�ӵ�����������
C���������2�����ӵ�ԭ�Ӷ��ǽ���ԭ��
D���������5�����ӵ�ԭ�Ӷ��Ƿǽ���ԭ��
�ο��𰸣�A
����������ǽ���Ԫ�أ�һ��������Ԫ�أ���������۵�����������������������A��ȷ��B�зǽ���Ԫ�ص���ͻ��ϼ۵ľ���ֵ�������γ�8�����ȶ��ṹ����ĵ�������Ҳ����8��ȥ������������Heԭ��������������ӣ���He���ǽ���������C���ڢ�A��Ԫ���е�Sb��Bi������㶼��5�����ӣ������Ƕ��ǽ�����D����
�����Ѷȣ���
4������� ��10�֣��±����г����ֶ�����Ԫ��A��B��C��D��E����Ϣ�����ƶϺ�����
Ԫ��
| �й���Ϣ
|
A
| Ԫ����Ҫ���ϼ�Ϊ ��2��ԭ�Ӱ뾶Ϊ0 .074 n m? .074 n m?
|
B
| ��������������������������֮��Ϊ4
|
C
| ԭ�Ӱ뾶Ϊ0.102 n m���䵥����A�ĵ�����ȼ�գ���������������ɫ����
|
D
| ����������ˮ����ܰ�1��1�������������ȵ�����������
|
E
| ԭ�Ӱ뾶Ϊ0.075 n m������������ˮ���������⻯�����һ����X
|
��1������B�����ӽṹʾ��ͼ?��д��DԪ������������ˮ�������ʽ?��
��2����Xˮ��Һ��?����ᡱ������С�)�ԣ������ӷ���ʽ������ԭ��?����3��D2CA3����Һ��B�ĵ����ܷ�����Ӧ���䷴Ӧ�����ӷ���ʽΪ?��
��4����֪EԪ�ص�ij���⻯��Y��A2��Ħ��������ͬ��Y�������ɵ�ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20��30����KOH��Һ����ȼ�ϵ�طŵ�ʱ�������ĵ缫��Ӧʽ��?��
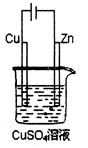
��5������ͼ��һ��������ʾ��ͼ������ʹ��Y������ȼ�ϵ����Ϊ�����̵�
��Դ��ͭƬ������ ��128g����Yһ����ȼ�ϵ�����������ı�״���µĿ�
��128g����Yһ����ȼ�ϵ�����������ı�״���µĿ�
������������������������Ϊ20����?L��
�ο��𰸣���10�֣�ǰ4���ո�1�֣���3���ո�2�֣�
��1��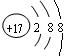 ?
?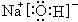 ?��2���ᣬNH4+��H2O
?��2���ᣬNH4+��H2O
 NH3��H2
NH3��H2 O��H+
O��H+
��3��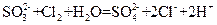 ?��4��
?��4��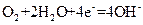 ?��5��112
?��5��112
�����������
�����Ѷȣ�һ��
5��ѡ���� ����˵������ȷ����
A.����Na2SO4��������Ͽ������������Σ�������������
B.����Na2SO4��Na2S��������Ͽ��������Կ������Σ��ֿ��Կ���������
C.ÿһ��Ԫ�ض�������һ���������Ե��ʻ������̬����
D.Ѫ�����ڻ����
�ο��𰸣�B
���������Na2S�������������������
�����Ѷȣ�����