1������� ��K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2��+7H2O��Ӧ�У�?����������??�ǻ�ԭ����?Ԫ�ر�������?Ԫ�ر���ԭ����0��3mol������������0��3mol��������ת�Ƶĵ�����ĿΪ?��
�ο��𰸣�K2Cr2O7; HCl; Cl; Cr; 0��6 NA����
���������K2Cr2O7��Cr�Ļ��ϼ���+6��ΪCrCl3�е�+3�����ϼ۽��ͣ�����ԭ������K2Cr2O7����������HCl��һ����Cl�Ļ��ϼ���-1��ΪCl2�е�0�����ϼ����ߣ����������ǻ�ԭ����������0��3mol������ת�Ƶĵ�����ĿΪ0��6 NA����
�����Ѷȣ�һ��
2������� ������ĺ���������ҽҩ�������ȷ���������Ҫ����;��
��1���ؾ�ʯ��BaSO4������θ������Ӱ����
��֪�������£�Ksp��BaSO4����1.1��10��10����BaSO4����Һ�м������ᣬ����Һ��pH��2ʱ����Һ��c��Ba2������?__��
��2����������茶���[��NH4��2Fe��SO4��2��6H2O]������������
�ټ��龧���к���NH4+�ķ���Ϊ?��
�ڵ����ʵ���Ũ�ȵ�����ϡ��Һ��
a����NH4��2Fe��SO4��2? b��NH4HSO4
c����NH4�� 2SO4?d����NH4��2SO3��
����c��NH4+���ɴ�С��˳��Ϊ?__����ѡ����ĸ����
��3����������أ�K2S2O8������ǿ��������Na2S2O3������ԭ����
��K2S2O8��Һ������MnSO4��Һ��ϣ��ڴ��������£����Թ۲쵽��Һ��Ϊ��ɫ���÷�Ӧ�����ӷ���ʽΪ?__��
���ò����缫�����H2SO4��K2SO4�Ļ����Һ�����Ʊ�K2S2O8���������ĵ缫��ӦʽΪ?__��������������������Һ��pH��?__���������С�����䡱����
�۲�Ʒ��K2S2O8�ĺ������õ������ⶨ����������Ϊ��ȡ0.3000 g��Ʒ�ڵ���ƿ�У���50 mLˮ�ܽ⣻����4.000 g KI���壨�Թ���������ʹ���ַ�Ӧ����������������Һ�ữ����?__Ϊָʾ������0.1000 mol��L��1 Na2S2O3��Һ�ζ����յ㣨��֪��I2��2S2O32-=2I����S4O62-�����ظ�2�Σ����ƽ�����ı�Һ21.00 mL���ò�Ʒ��K2S2O8����������Ϊ�����ʲ��μӷ�Ӧ��?__����ʽ�����㣩��
�ο��𰸣���1��2.2��10��8mol/L
��2����ȡ�������壬��ˮ�ܽ⣬�ټ�������NaOHŨ��Һ���ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬����NH4+
��a��c��d��b
��3����5S2O82-��2Mn2����8H2O 10SO42-��2MnO4-��16H��
10SO42-��2MnO4-��16H��
��2SO42-��2e��=S2O82-����2HSO4-��2e��=S2O82-��2H����������
�۵���?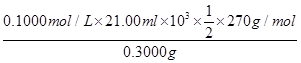
��100%��94.50%
�����������1��Ksp��c��Ba2������c��SO42-��������c��Ba2������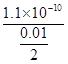 mol/L��2.2��10��8mol/L����2����������ʵ���Ũ�ȣ�����b��С��a����Ƶ�˫ˮ�⡢c��ˮ�⡢d��ٽ���˫ˮ�⣬����c��NH4+����a��c��d��b����3������Һ��Ϊ��ɫ˵��������MnO4-��������ʧ���ӻ��ϼ����ߣ�2SO42-��2e��=S2O82-������H���ŵ磬ˮ�ĵ���ƽ�������ƶ���c��OH��������K2S2O8����ǿ�����Կ��Խ�I������ΪI2������ָʾ��ѡ����ۣ���S2O82-��2I��=2SO42-��I2��I2��2S2O32-=2I����S4O62-���ù�ϵn��S2O82-����2n��S2O32-����
mol/L��2.2��10��8mol/L����2����������ʵ���Ũ�ȣ�����b��С��a����Ƶ�˫ˮ�⡢c��ˮ�⡢d��ٽ���˫ˮ�⣬����c��NH4+����a��c��d��b����3������Һ��Ϊ��ɫ˵��������MnO4-��������ʧ���ӻ��ϼ����ߣ�2SO42-��2e��=S2O82-������H���ŵ磬ˮ�ĵ���ƽ�������ƶ���c��OH��������K2S2O8����ǿ�����Կ��Խ�I������ΪI2������ָʾ��ѡ����ۣ���S2O82-��2I��=2SO42-��I2��I2��2S2O32-=2I����S4O62-���ù�ϵn��S2O82-����2n��S2O32-����
�㲦�����⿼�����ӷ�Ӧ�����鿼���ۺϷ���������������Ѷ��еȡ�
�����Ѷȣ�һ��
3������� ��1������ɴ��ϵ�����ȼ�ϵ�أ����ط�ӦΪ��2H2+O2=2H2O��д���������Һ��Ϊ����ʱ��������Ӧʽ��______��
��2����֪4g����������ȼ������CO2�����壩��H2O��Һ��ʱ���ų�Q?kJ��������д������ȼ���ȵ��Ȼ�ѧ����ʽ��______��
��3����ƽ��
______Na2SO3+______KIO3+______H2SO4��______Na2SO4+______K2SO4+______I2+______H2O��
�ο��𰸣���1�������õ��ӱ���ԭ�������õ��Ӻ���Һ�е������ӷ�Ӧ����ˮ�����Ե缫��ӦʽΪO2+4H++4e-�T2H2O��
�ʴ�Ϊ��O2+4H++4e-�T2H2O��
��2��4g����������ȼ������CO2�����壩��H2O��Һ��ʱ���ų�Q?kJ��������1mol������ȼ������CO2�����壩��H2O��Һ��ʱ���ų�4Q?kJ��������������ȼ���Ȼ�ѧ��Ӧ����ʽΪ��
CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-4QKJ/mol��
�ʴ�Ϊ��CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=-4QKJ/mol��
��3��һ�������������ʧȥ2������������������ӣ�����KIO3���ӵõ�10����������һ��I2���ӣ����Ե�ʧ���ӵ���С������Ϊ10�����������Ƶļ�����Ϊ5������صļ�����Ϊ2��Ȼ�����ԭ���غ���ƽ���ɣ�
���Է���ʽΪ��5Na2SO3+2KIO3+H2SO4=5Na2SO4+K2SO4+I2+H2O��
�ʴ�Ϊ��5��2��1��5��1��1��1��
���������
�����Ѷȣ�һ��
4������� (16��)������������(Na2S2O4)���ֳƱ��շۣ���ӡˢ��ҵ����Ҫ�Ļ�ԭ����ij����С���������ʵ�飺
I�����������ϡ�
��1��������������(Na2S2O4)��һ�ְ�ɫ��ĩ��������ˮ���������Ҵ���
��2��2Na2S2O4��4HCl= 4NaCl��S����3SO2����2H2O��Na2S2O3��2HCl= 2NaCl��S����SO2����H2O��
II�����Ʊ�������
75��ʱ�������ƺʹ�������Ҵ�ˮ��Һ�У�ͨ��SO2���з�Ӧ������䷴Ӧ����ʽ��

��ȴ��40��50�棬���ˣ��� ϴ�ӣ������Ƶ�Na2S2O4��
III����Na2S2O4�����ʡ�
��1��Na2S2O4��Һ�ڿ������ױ�����������С��ⶨ0.050mol/L
Na2S2O4��Һ�ڿ�����pH�仯��ͼ��ʾ��0��t1����Ҫ������HSO3��������pH�仯ͼ��HSO3���ĵ���̶� ˮ��̶�(���������)��
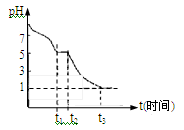
����С���Ʋ�Na2S2O4��Һ�ڿ������ױ�������0��t1�η������ӷ�Ӧ����ʽΪ ��t3ʱ��Һ����Ҫ�����ӷ����� ��
��2��������������Na2S2O4������ȫ�ֽ⣬�õ��������Na2SO3��Na2S2O3������Ϊ (�ѧʽ)��
�������ʵ����֤������Na2S2O3���ڣ�����±������ݡ�
(��ѡ����Լ���ϡ���ᡢϡ���ᡢBaCl2��Һ��KMnO4��Һ)
ʵ�鲽��(��Ҫ��д�������������)
| Ԥ�ڵ�ʵ������ͽ���
|
|
|
�ο��𰸣�(16�֣�ÿ��2��) II��2HCOONa��Na2CO3��4SO2= 2Na2S2O4��3CO2��H2O �Ҵ�
III����1�� �� 2S2O42����O2��2H2O=4HSO3�� SO42��(��HSO4��) ��2�� SO2
ʵ�鲽��(��Ҫ��д�������������)
Ԥ�ڵ�ʵ������ͽ���
ȡ������ȫ�ֽ�Ĺ���������Թ��У�����ϡ����(2��)
���е���ɫ����������Na2S2O3����(2��)
���������II����Ӧ��SԪ�صĻ��ϼ۴�+4�۽��͵�+3�ۣ��õ�1�����ӡ���������̼Ԫ�صĻ��ϼ۴�+2�����ߵ�+4�ۣ�����ݵ��ӵ�ʧ�غ��ԭ���غ��֪��Ӧ�Ļ�ѧ����ʽΪ2HCOONa��Na2CO3��4SO2= 2Na2S2O4��3CO2��H2O��������������(Na2S2O4)��һ�ְ�ɫ��ĩ��������ˮ���������Ҵ�����˿������Ҵ�ϴ�Ӳ�Ʒ��
III����1��0��t1����Ҫ������HSO3��������ͼ���֪��Һ�����ԣ���˵��HSO3���ĵ���̶ȴ���ˮ��̶ȡ�
Na2S2O4��Һ�ڿ������ױ������������������ƣ���0��t1�η������ӷ�Ӧ����ʽΪ2S2O42����O2��2H2O=4HSO3����t3ʱ��Һ��pH��1��˵����Һ�����Խ�ǿ��������������Ʊ�����Ϊ�������ƣ�����Һ����Ҫ�����ӷ�����SO42����
��2��������������Na2S2O4������ȫ�ֽ⣬�õ��������Na2SO3��Na2S2O3�����壬�����������������������Na2S2O3��S��+2�ۣ������������ԭ��Ӧ�е��ӵ�ʧ�غ��֪����Ӧ����SO2�����ݷ�ӦNa2S2O3��2HCl= 2NaCl��S����SO2����H2O��֪Ҫ������������ƣ���ֻ��Ҫȡ������ȫ�ֽ�Ĺ���������Թ��У�����ϡ���ᣬ����е���ɫ����������Na2S2O3���ڡ�
���㣺����������ԭ��Ӧ��ˮ�ⷴӦ�������Ʊ��ͼ���ʵ�������̽��
�����Ѷȣ�����
5������� ��10�֣���ҵ����MnO2��KOHΪԭ����ȡ������أ���Ҫ�������̷��������С���һ����MnO2����KOH���飬��Ͼ��ȣ��ڿ����м������ۻ������������裬��ȡK2MnO4���ڶ�����K2MnO4��Ũ��Һ���е�⣬��ȡKMnO4���Իش��������⣺
��1����ȡK2MnO4��MnO2����һ������ԭ��Ӧ��_____________�������������ԭ���������������Ŀ����________________________________��
��2�����K2MnO4��Ũ��Һʱ�����������ĵ缫��ӦʽΪ��
������_______________________,
������_________________________��
����ܵķ�Ӧ����ʽ��_________________________��
�ο��𰸣���10�֣�ÿ��2�֣���1����ԭ�����������ֽӴ���ʹMnO2������ȫ
��2��2H++2e-==H2����MnO42��-e-="==" MnO4-,2K2MnO4+2H2O==2KMnO4+2KOH+ H2��
�����������
�����Ѷȣ�һ��