1、填空题 在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中,?是氧化剂,??是还原剂,?元素被氧化,?元素被还原,若0.3mol氯气生成则若0.3mol氯气生成转移的电子数目为?。
2、填空题 许多硫的含氧酸盐在医药、化工等方面有着重要的用途。
(1)重晶石(BaSO4)常做胃肠道造影剂。
已知:常温下,Ksp(BaSO4)=1.1×10-10。向BaSO4悬浊液中加入硫酸,当溶液的pH=2时,溶液中c(Ba2+)=?__。
(2)硫酸亚铁铵晶体[(NH4)2Fe(SO4)2・6H2O]常做分析剂。
①检验晶体中含有NH4+的方法为?。
②等物质的量浓度的四种稀溶液:
a.(NH4)2Fe(SO4)2? b.NH4HSO4
c.(NH4) 2SO4?d.(NH4)2SO3,
其中c(NH4+)由大到小的顺序为?__(填选项字母)。
(3)过二硫酸钾(K2S2O8)常做强氧化剂,Na2S2O3常做还原剂。
①K2S2O8溶液与酸性MnSO4溶液混合,在催化剂作用下,可以观察到溶液变为紫色,该反应的离子方程式为?__。
②用铂做电极,电解H2SO4和K2SO4的混合溶液可以制备K2S2O8,其阳极的电极反应式为?__,电解过程中阴极附近溶液的pH将?__(填“增大”“减小”或“不变”)。
③产品中K2S2O8的含量可用碘量法测定。操作步骤为称取0.3000 g产品于碘量瓶中,加50 mL水溶解;加入4.000 g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以?__为指示剂,用0.1000 mol・L-1 Na2S2O3标准液滴定至终点(已知:I2+2S2O32-=2I-+S4O62-)。重复2次,测得平均消耗标准液21.00 mL。该产品中K2S2O8的质量分数为(杂质不参加反应)?__(列式并计算)。
3、简答题 (1)宇宙飞船上的氢氧燃料电池,其电池反应为:2H2+O2=2H2O试写出电解质溶液若为盐酸时的正极反应式:______.
(2)已知4g甲烷气体充分燃烧生成CO2(气体)和H2O(液)时,放出Q?kJ的热量.写出甲烷燃烧热的热化学方程式:______.
(3)配平:
______Na2SO3+______KIO3+______H2SO4→______Na2SO4+______K2SO4+______I2+______H2O.
4、填空题 (16分)连二亚硫酸钠(Na2S2O4),又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验:
I.【查阅资料】
(1)连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇。
(2)2Na2S2O4+4HCl= 4NaCl+S↓+3SO2↑+2H2O;Na2S2O3+2HCl= 2NaCl+S↓+SO2↑+H2O。
II.【制备方法】
75℃时将甲酸钠和纯碱加入乙醇水溶液中,通入SO2进行反应,完成其反应方程式:

冷却至40~50℃,过滤,用 洗涤,干燥制得Na2S2O4。
III.【Na2S2O4的性质】
(1)Na2S2O4溶液在空气中易被氧化.课题小组测定0.050mol/L
Na2S2O4溶液在空气中pH变化如图所示:0~t1段主要先生成HSO3-,根据pH变化图,HSO3-的电离程度 水解程度(填“<”或“>”)。
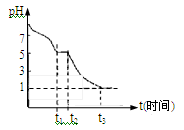
课题小组推测Na2S2O4溶液在空气中易被氧化,0~t1段发生离子反应方程式为 。t3时溶液中主要阴离子符号是 。
(2)隔绝空气加热Na2S2O4固体完全分解,得到固体产物Na2SO3、Na2S2O3和气体为 (填化学式).
请你设计实验验证产物有Na2S2O3存在,完成下表中内容。
(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、KMnO4溶液)
实验步骤(不要求写出具体操作过程)
| 预期的实验现象和结论
|
|
|
5、填空题 (10分)工业上用MnO2和KOH为原料制取高锰酸钾,主要生产过程分两步进行。第一步将MnO2和固体KOH粉碎,混合均匀,在空气中加热至熔化,并连续搅拌,制取K2MnO4;第二步将K2MnO4的浓溶液进行电解,制取KMnO4。试回答以下问题:
(1)制取K2MnO4的MnO2是这一氧化还原反应的_____________剂(填“氧化”或“还原”),连续搅拌的目的是________________________________。
(2)电解K2MnO4的浓溶液时,两极发生的电极反应式为:
阴极是_______________________,
阳极是_________________________,
电解总的反应方程式是_________________________。