ϡ��ˮ
�ο��𰸣�C
���������Aѡ���������ܳ�ȥSO23-����Ӱ��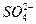 �ļ��顣Bѡ����AgClΪ��ɫ������AgIΪ��ɫ��������Cl-�Ĵ��ڲ�Ӱ��I-�ļ��顣Cѡ����Fe3+��SCN-��Ӧʹ��Һ��Ѫ��ɫ������Fe2+�ļ��顣Dѡ���а�ˮ����ʱAg+תΪ��Ag��NH3��2��+��Al3+ת��ΪAl��OH��3��ɫ��������Ag+�Ĵ��ڲ�Ӱ��Al3+�ļ��顣 �ļ��顣Bѡ����AgClΪ��ɫ������AgIΪ��ɫ��������Cl-�Ĵ��ڲ�Ӱ��I-�ļ��顣Cѡ����Fe3+��SCN-��Ӧʹ��Һ��Ѫ��ɫ������Fe2+�ļ��顣Dѡ���а�ˮ����ʱAg+תΪ��Ag��NH3��2��+��Al3+ת��ΪAl��OH��3��ɫ��������Ag+�Ĵ��ڲ�Ӱ��Al3+�ļ��顣
�����Ѷȣ���
2��ѡ���� �����ĸ���ѧ��Ӧ�У����ϴ������龰���ǣ�?��?

A��H2��CuO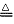 Cu��H2O Cu��H2O
B��CuO��CO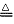 Cu��CO2 Cu��CO2
C��Fe��H2SO4��FeSO4��H2��
D��Fe��CuSO4��FeSO4��Cu
�ο��𰸣�D
�����������
�����Ѷȣ���
3�������� ��12.8����CuSO4��Fe��ɵĹ��壬����������ˮ�г�ַ�Ӧ���˳����壬�����Ƶ�5.2�ˡ���ԭ�������CuSO4��Fe��Ϊ���ٿˣ�
�ο��𰸣�CuSO4Ϊ8�ˣ�FeΪ4.8��
������������������ַ�Ӧ���ܣ�ǡ����ȫ��Ӧ��CuSO4������Fe������
���¹����������ܣ�(1)����Fe��Cu��(2)����ȫ��Cu.
(1)�����¹�����Fe��Cu(��Fe����)ʱ����x��CuSO4�ľ�������Ϊ(12.8-x)�ˣ��û�����Ϊ5.2-(12.8-x)�ˡ�
CuSO4 + Fe 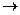 ?FeSO4 +Cu?�������� ?FeSO4 +Cu?��������
160? 56? 64? 64-56=8(���۲���)
x? 5.2-(12.8 -x)(ʵ�ʲ���) -x)(ʵ�ʲ���)
160:x=8:[5.2-(12.8-x)]
��? x=8(��)��12.8-x=4.8(��)��
(2)�����¹���ȫ��Cu����Ӧʱ��w��Fe�ľ���
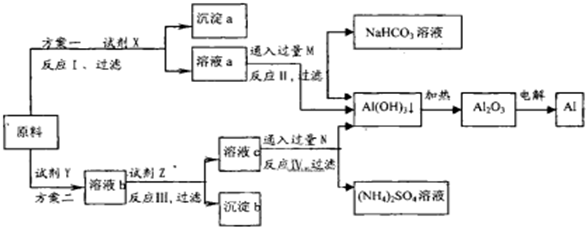
CuSO4 + Fe 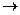 ?FeSO4+ Cu?�������� ?FeSO4+ Cu?��������
56? 64? 64-56=8(���۲���)
 ?W? 5.2-w(ʵ�ʲ���) ?W? 5.2-w(ʵ�ʲ���)
56:w=8:5.2-w
��? w=4.55(��)��
��ԭ�������CuSO4Ϊ12.8-4.55=8.25(��)��
��8.25��CuSO4��ֻ��8.25�� =3.3(��)Cu���ʲ�������5.2��Cu���ɡ��ɴ˿ɼ�(2)�ļ��費������ =3.3(��)Cu���ʲ�������5.2��Cu���ɡ��ɴ˿ɼ�(2)�ļ��費������
�����Ѷȣ���
4������� ij�о���ѧϰС���ò�����������������ΪFe2O3��Ϊԭ�ϣ������ұ���������¹������̣����ַ�Ӧ����û�б������
��1���Լ�X�Ļ�ѧʽΪ______����ӦI�����ӷ���ʽ��______��
ʵ��������480mL?1mol?L-1?X����Һ�����õ������������ձ������������Լ�ƿ����ͷ�ι��⣬����______�����������Ա궨����X����ҺŨ���Ƿ�ȷ��ʵ��������______��
��2�����շ�����ƣ��Լ�Z�������ǵ�����Һ��pH�������ɳ���b[Fe��OH��3]����ʵ�ʹ�ҵ�ĽǶȣ�����Ϊ����______��������������______
��3����֪NΪ������ʵ�����л���������ͼװ����ȡ���������а�����Ȫʵ�飮
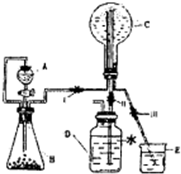
������A��������______��װ����A�ڲ���B�ڲ�֮����ͨ�����ܵ�������______
�����ô�װ���Ʊ�N������A��ʢ��Ũ��ˮ����Bװ���еĹ����Լ�������ѡ�����е�______������ĸ��ţ���
A����ʯ��?B���ռ�?C������?D����ʯ��
��4����D�����ȵ���������̪����C��Һ���______ɫ�������ӷ���ʽ����ԭ��______��
�ο��𰸣���1������һ������Һaͨ�������M������������������̼�����ƿ�֪����Һa�к���ƫ�����������MΪ������̼�����Լ�XΪNaOH��Һ����ӦIΪ������������������Һ��Ӧ����ƫ��������ˮ�����ӷ���ʽΪ��Al2O3+2OH-�T2AlO2-+H2O��
ʵ����û��480mL����ƿ��Ӧѡ��500mL����ƿ������500mL1mol?L-1?NaOH����Һ��Ҫ���������У��ձ������������Լ�ƿ����ͷ�ιܡ�500mL����ƿ����ȱ��500mL����ƿ��
���������к͵ζ������Ա궨����NaOH��ҺŨ���Ƿ�ȷ��
�ʴ�Ϊ��NaOH��Al2O3+2OH-�T2AlO2-+H2O��500mL����ƿ���к͵ζ���
��2��������������Һcͨ�������N����������������������刺�֪����Һc�к��������ӡ�NΪ���������Լ�YΪ���ᣬ��Һb�к�����������������������PHֵ����������ת��Ϊ�������������˺�������Һ�м�������İ�ˮ���������ӣ�
�뷽��һ��Ƚϣ�����һ�����٣��������ʷ���һ��������
�ʴ�Ϊ������һ�������٣�������
��3���١�����A�Ƿ�Һ©����װ����A�ڲ���B�ڲ�֮����ͨ�����ܵ������ǣ�ƽ���Һ©������ѹǿ����ֹ��Һ©��������
�ڡ�A��ʢ��Ũ��ˮ������ʯ�ҡ��ռ��ʯ�һ�ϣ��ų��������ȣ���Һ������������Ũ���������ð����ݳ������������İ�������ˮ�뵨����Ӧ����������ͭ���������ܲ�����������C���ܿ��ԣ�
�ʴ�Ϊ��C��
��4����������ˮ����Ӧ����һˮ�ϰ���һˮ�ϰ��������������NH3+H2O?NH3?H2O?NH4++OH-����Һ�ʼ��ԣ���̪�ڼ��������³ʺ�ɫ��
�ʴ�Ϊ���죻NH3+H2O?NH3?H2O?NH4++OH-��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ij�����ˮ��Һ�м��뺬Fe2+����Һ�������Ա仯�����μӼ�����ˮ���Һ���ֺ�ɫ����ô�ɴ˵ó������н��ۣ��������
[? ]
A���þ�����һ������SCN-
B��Fe3+�������Ա�Br2��������ǿ
C��Fe2+��Br2����ΪFe3+
D��Fe2+��SCN-�����γɺ�ɫ�Ļ�����
�ο��𰸣�B
���������
�����Ѷȣ���
|