1������� ZnO���п�����,Ҳ����Ҫ����̥���Ӽ�����ҵ���ɴ�ZnO����FeO��CuO���Ʊ�����ZnO�������£�
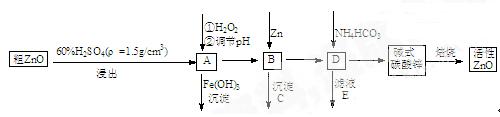
��֪����Һ��Fe2+�� Fe3+��? Cu2+?�� Zn2+�γ����������pH���±�
����
| ��ʼ��������pH
| ��ȫ������pH
|
Fe2+
| 6.4
| 8.4
|
Fe3+
| 2.4
| 3.1
|
Cu2+
| 5.2
| 6.7
|
Zn2+
| 6.8
| 9
|
��1��ʵ��������98��H2SO4������ϡ��������ʹ�õIJ��������У���ͷ�ιܡ�_______��_______��_______��
��2����A�м�H2O2��Ŀ��֮һ��ʹ��ҺpH���ߣ�ʹFe3+������ȫ�������һ��Ŀ����?����A��?(��ܡ����ܡ�)ʹFe2+ֱ�ӳ�����ȥ;
��3��ҪʹA��Һ˳����ΪB��Һ, ��Һ��pHӦ������??;? B�м���Zn�����ܽ���������Ũ������?��
��4����д��ʽ̼��п�����Ʊ�����ZnO�Ļ�ѧ����ʽ?.
�ο��𰸣�
�����������
�����Ѷȣ�һ��
2������� I. ��������8������
��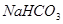 ����
����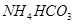 ����
���� ����HF����
����HF����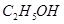 ����
����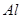 ����ʳ��ˮ����
����ʳ��ˮ����
��������ǿ����ʵ���_____________������ţ���ͬ�������ܸ����ᷴӦ���ܸ�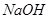 ��Һ��Ӧ����_____________��
��Һ��Ӧ����_____________��
II. ����һƿŨ��Ϊ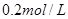 ��ij����Һ������Ϊ���ᡢ���ᡢ�����е�һ�֣�Ϊ��ȷ��������Һ����ɽ���ʵ�飺ȡ
��ij����Һ������Ϊ���ᡢ���ᡢ�����е�һ�֣�Ϊ��ȷ��������Һ����ɽ���ʵ�飺ȡ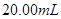 ����
���� ��Һ����μ���
��Һ����μ���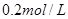 ������������Һ��ǡ�÷�Ӧ��ȫʱ�����Һ���Ϊ
������������Һ��ǡ�÷�Ӧ��ȫʱ�����Һ���Ϊ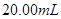 �����û�ѧ����ش�
�����û�ѧ����ش�
��1�����������____________��
��2����pH��ֽ��÷�Ӧ��������Һ�ʼ��ԣ����ݴ�����˵��������ҺΪ____________�������ӷ���ʽ˵����Һ�ʼ��Ե�ԭ��_________ _______________��
_______________��
III. A��B��C��D��Ϊ������ˮ�Ĺ��壬������ǵ������У�
?�ֱ�ȡ���ǵ�ˮ��Һ����ʵ�飬��� ���£�
���£�
��A��B��Ӧ���ɰ�ɫ�������ټӹ���A�����������٣���������ʧ��
��C��D��Ӧ�к��ɫ�������ɲ��ų����塣
��B��C��Ӧ�а�ɫ�������ɲ��ų����塣
��1��д�����ǵĻ�ѧʽ��A___________��B___________��C___________��D___________��
��2��д������B��C��Ӧ�����ӷ���ʽ_________________________________��
�ο��𰸣�I. �٢ڢ�?�٢ڢ�
II. ��1�� ?��2��
?��2��


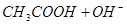
III. ��1�� ?
?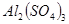 ?
? ?
?
��2��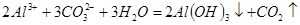
�����������
�����Ѷȣ�һ��
3��ʵ���� ��4�֣���ͼ��ʾ����һ�ձ���ʢ��H2SO4��Һ�� ͬʱ��һ����⻬������С����������Һ���룬����ձ��л���ע����H2SO4��ҺͬŨ�ȵ�Ba(OH)2��Һ��ǡ����ȫ��Ӧ���Իش��������⣺
ͬʱ��һ����⻬������С����������Һ���룬����ձ��л���ע����H2SO4��ҺͬŨ�ȵ�Ba(OH)2��Һ��ǡ����ȫ��Ӧ���Իش��������⣺
 ��1����ʵ���У��۲쵽��������
��1����ʵ���У��۲쵽��������
��?��?
��?��
��2��д����ʵ���з�Ӧ�����ӷ���ʽ?
?��
�ο��𰸣���1����Һ���а�ɫ������������2��С���³����ձ��ף���3��Ba2++2OH-+2H++SO42- =BaSO4��+4H2O��
�������������Ba(OH)2��Һ��ע�룬����H2SO4��Һ��Ӧ���ɳ�����������Һ��Ũ��Խ��ԽС��С���ܵ��ĸ�����С�����ջ�ʹС���³����ձ��ס�
�����Ѷȣ���
4��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ����
A.�ö��Ե缫���MgCl2��Һ��2Cl-+2H2O�TCl2��+H2��+2OH-
B.���Ʒ���ˮ�⣺S2-+H2O=HS-+OH-
C.����С�մ���Һ����Ba��OH��2��Һ�У�HCO-3ʮBa2++OH-=BaCO3��+H2O
D.��NH4HSO4��Һ�м���NaOH��Һ�����ҺΪ���ԣ�H++OH-=H2O
�ο��𰸣�C
����������������������ӷ���ʽ��дҪ�����жϣ��翴�Ƿ��غ㣨��������ɡ���ʧ���ӣ����Ƿ���Ͽ���ʵ����ѧʽ��֡���ѧ����ʹ���Ƿ���ȷ����Ӧ���������䷴Ӧ�Ƿ�һ�£��Ƿ�����������ӵȣ�
���A������ʱ���������������˴���OH-��OH-����Mg2+��Ӧ��Mg2++2OH-=Mg��OH��2������A����
B����ˮ�ⷴӦΪ���淴Ӧ��S2-��ˮ���á�?�������á�=������B����
C����HCO-3+OH-=CO32-+H 2O����������С�մ���Һ����Ba��OH��2��Һ�з���NaHCO3+Ba��OH��2=BaCO3��+H2O+NaOH����C��ȷ��
D����NH4HSO4��Һ��NH+4��OH-��Ӧ��NH+4+OH-=NH3?H2O����D����
��ѡC��
���������⿼�������ӷ���ʽ�����жϵķ�����ֻҪ����һЩ�������жϷ������Ϳ�������ӭ�ж����ˣ�
�����Ѷȣ�һ��
5��ѡ���� ��������������Һ���ܴ����������
A.Fe3+��SCN����I����K+
B.K+��Al3+��SO42����MnO4��
C.H+��NO3����Fe2+��Na+
D.Cu2+��NH4+��Br����OH��
�ο��𰸣�B
���������������������������������������������ɫ��Ӧ�������ӻ������������ӣ���Aѡ�����K+��Al3+��SO42����MnO4��֮�䲻�ܷ�Ӧ����Bѡ����ȷ�������������������������ױ������������������Cѡ�����ͭ��������������������Ӧ����������ͭ������笠���������������������Ӧ����һˮ�ϰ�������ˮ����Dѡ�����
���㣺�������ӹ��棬��Ҫ�漰����֮�䷴Ӧ����������ѵ�������ӷ��������ԭ��Ӧ����ɫ��Ӧ����ˮ�ⷴӦ�ȡ�
�����Ѷȣ�һ��