1��ѡ���� ��m mol A ��n mol B ����һ�ܱ������У�������Ӧ���£�m A(g) + n B(g)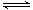 p C(g)����H = a kJ/mol ( a<0)�����ں��¡������´ﵽƽ��ʱA��ת����ΪA1% ���ھ��ȡ����������´ﵽƽ��ʱA��ת����ΪA2%����A1��A2�Ĺ�ϵΪ
p C(g)����H = a kJ/mol ( a<0)�����ں��¡������´ﵽƽ��ʱA��ת����ΪA1% ���ھ��ȡ����������´ﵽƽ��ʱA��ת����ΪA2%����A1��A2�Ĺ�ϵΪ
A��A1<A2
B��A1=A2
C��A1>A2
D������ȷ��
2��ѡ���� ����˵����ȷ���ǣ�?��
A����ѧ��Ӧ�л�ѧ��ֻ����ת��Ϊ����
B�����淴Ӧ�ﵽƽ��������淴Ӧ���ʾ�Ϊ0
C��N?2��H2��Ӧ�ﵽƽ�����N?2��H2ʣ��
D����ѧ��Ӧ��һ���л�ѧ���Ķ��Ѻ��γ�
3�������� �������ʵ�����A��B�����2L���ܱ������У�������Ӧ��3A(g)+B(g)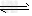 xC(g)?+2D(g)����5?min���D��Ũ��Ϊ0.5?mol/L��c(A)��c(B)=3��5��C��ƽ����Ӧ������0.1?mol/(L
xC(g)?+2D(g)����5?min���D��Ũ��Ϊ0.5?mol/L��c(A)��c(B)=3��5��C��ƽ����Ӧ������0.1?mol/(L min)����
min)����
(1)��Ӧ��ʼǰ���������е�A��B�����ʵ�����
(2)x��ֵ��
(3)B��ƽ����Ӧ���ʡ�
4��ѡ���� ��2.0molPCl3����1.0molCl2�������������ܱ������У���һ�������·���������Ӧ��PCl3(g)+Cl2(g)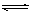 PCl5(g)�ﵽƽ��ʱ,PCl5Ϊ0.40mol�������ʱ����1.0molPCl3��0.50molCl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ�����
PCl5(g)�ﵽƽ��ʱ,PCl5Ϊ0.40mol�������ʱ����1.0molPCl3��0.50molCl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ�����
A��0.40mol
B����0.20mol
C��0.20mol
D������0.20mol����0.40mol
5������� ��10�֣�ֱ���ŷź�SO2���������γ����꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2��
��1���û�ѧ����ʽ��ʾS�γ���������ķ�Ӧ����ʽ����������������������������
��2�����Ƽ�ѭ�����У�Na2SO3��Һ��Ϊ����Һ������NaOH��Һ����SO2�Ƶã��÷�Ӧ�����ӷ���ʽ��?��
��3������Һ����SO2�Ĺ����У�pH��n(SO3?��)��n(HSO3��)�仯��ϵ���±�:
n(SO3?��):��n(HSO3��)
| 91��9
| 1��1
| 1��91
|
PH
| ��.��
| 7.2
| 6.2
|
���ϱ��ж�NaHSO3��Һ���������������ԣ��û�ѧƽ��ԭ������:��������������������������
�ڵ�����Һ������ʱ����Һ������Ũ�ȹ�ϵ��ȷ����(ѡ����ĸ):������������������������
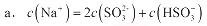

��4��������Һ��pH����ԼΪ6ʱ��������������������ʾ��ͼ����:

��HSO3-�������ŵ�ĵ缫��Ӧʽ����������������������������������
�ڵ�����������ҺPH����8����ʱ������Һ������ѭ�����á���������ԭ��:����������������
������������������������