1、简答题 通过金属与盐溶液的置换反应可以比较金属还原性的强弱,通过非金属间的置换反应,也可以比较非金属氧化性的强弱.
实验一:说明氯的氧化性强于碘.
Ⅰ.向盛有KI溶液的试管中加入少许CCl4后,滴加新制氯水,振荡,CCl4层变成紫色.
用离子方程式表示CCl4层变紫色的原因______
Ⅱ.如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色.
CCl4层最后变成无色的原理如下,完成并配平该反应:
____________+______I2+____________→______HIO3+____________
Ⅲ.氯的非金属性比碘强,用原子结构解释原因:______,
原子半径逐渐增大,得电子能力逐渐减弱.
实验二:说明氯元素的氧化性强于氮元素
下面装置(烧瓶内已无空气)能实现Cl2置换N2的反应,请回答:
通入?Cl2?后:
Ⅰ.现象一:烧瓶中会出现白烟.白烟的成分是______.
Ⅱ.现象二:形成喷泉,NaOH溶液进入烧瓶.烧瓶内压强减小的原因是______.?写出NaOH在烧瓶内发生反应的离子方程式______
Ⅲ.除上述现象外,能说明有N2产生的实验现象是______.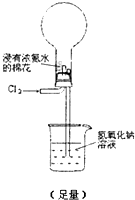
参考答案:实验一:
Ⅰ.氯水中含有氯气,氯气和碘离子能发生置换反应生成碘单质,离子方程式为:2I-+Cl2=I2+2Cl-,碘在四氯化碳中的溶解度大于在水中的溶解度,且碘和四氯化碳不反应,四氯化碳和水不互溶,所以四氯化碳能萃取碘水中的碘,碘在四氯化碳中呈紫红色,故答案为:2I-+Cl2=I2+2Cl-;
Ⅱ.氯气具有强氧化性,能氧化碘单质生成碘酸,同时自身被还原生成氯化氢,该反应中氯元素化合价由0价变为-1价,碘元素化合价由0价变为+5价,所以其转移电子数是10,再结合原子守恒配平方程式,所以反应方程式为:5Cl2+I2+6H2O=2HIO3+10HCl,故答案为:5Cl2+I2+6H2O=2HIO3+10HCl;
Ⅲ.同主族元素从上到下,原子核外电子数增多,原子核吸引电子的能力降低,则得电子能力逐渐减弱,故答案为:同主族元素从上到下原子核外电子层数依次增多;
实验二:Ⅰ.氯气和氨气反应生成氮气和氯化铵,氯化铵是固体所以是白烟,故答案为:NH4Cl;
Ⅱ.氨气和氯气反应生成氯化铵和氮气,反应前后气体的物质的量减小,所以压强减小,烧碱溶液进入烧瓶,氨水中铵根离子和氢氧根离子反应生成一水合氨,离子反应方程式为:NH4++OH-?NH3?H2O;氯气和氢氧根离子反应,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:烧瓶内发生反应8NH3(g)+3?Cl2(g)=N2(g)+6NH4Cl(s),气体大量减少,烧瓶内压强低于大气压,NH4++OH-?NH3?H2O;Cl2+2OH-=Cl-+ClO-+H2O;
Ⅲ.氮气和水不反应,所以在烧瓶内要占有部分空间,导致溶液不能充满烧瓶,故答案为:液体不能充满烧瓶.
本题解析:
本题难度:一般
2、推断题 现有A、B、C、D、E五种元素,A的原子核中没有中子,B、C元素处于同一周期,C的原子半径较小,B、C的质子数之和为27,质子数之差为5;2.7g D的单质跟足量的盐酸反应,生成D3+和3.36L(标准状况)氢气;E和C能形成E2C型离子化合物,且E、C两元素的简单离子具有相同的电子层结构。
(1)写出元素符号:A ___________,B___________,E___________;
(2)D与盐酸反应的离子方程式为:______________________;
(3)C的原子结构示意图为:___________,A与C形成的化合物的电子式为______________________,该化合物含有的化学键为___________(填“离子键”或“共价键”), C的其中一种氧化物能与O2在一定温度和有催化剂存在的条件下反应,该反应的化学方程式______________________;
(4)用电子式表示C与E形成E2C的过程:_________________________________。
参考答案:(1)H;Na;K
(2)2Al+6H+==2Al3++3H2↑
(3)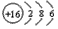 ;
;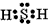 ;共价键;2SO2+O2
;共价键;2SO2+O2 2SO3
2SO3
(4)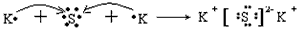
本题解析:
本题难度:一般
3、选择题 下列各组中化合物的性质比较,不正确的是( )
A.酸性:HClO4>HBrO4>HIO4
B.碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
C.稳定性:HCl>H2S>PH3
D.还原性:F->Cl->Br-
参考答案:A.非金属性Cl>Br>I,对应元素的最高价氧化物的水化物的酸性为HClO4>HBrO4>HIO4,故A正确;
B.金属性为Ba>Ca>Ba,则对应元素的最高价氧化物的水化物的碱性为Ba(OH)2>Ca(OH)2>Mg(OH)2,故B正确;
C.非金属性Cl>S>P,则气态氢化物的稳定性为HCl>H2S>PH3,故C正确;
D.非金属性F>Cl>Br,对应离子的还原性为F-<Cl-<Br-,故D错误;
故选D.
本题解析:
本题难度:简单
4、选择题 甲、乙是周期表中同一主族的两种元素,若甲的原子序数为X,则乙的原子序数不可能是
[? ]
A.X+2
B.X+4
C.X+8
D.X+18
参考答案:B
本题解析:
本题难度:简单
5、选择题 青花瓷,俗称青花,是中国瓷器的主流品种之一。某同学利用如下方法来粗略测定如图所示的青花瓷瓶的容积。把32.76 g NaCl晶体放入到500 ml烧杯中,加入200 ml蒸馏水,待NaCl完全溶解后,将溶液全部转移到该瓶中,用蒸馏水稀释至完全充满容器。从中取出100 ml溶液,该溶液恰好能与10 ml.0.100 mol / L的AgNO3溶液完全反应。则下列说法正确的是?(?)

A.该青花瓷瓶的容积约为5.6 L
B.常温下,该青花瓷瓶几乎能容纳56 kg H2O
C.常温常压下,该青花瓷瓶几乎能容纳70 g N2
D.青花为高级瓷器,该青花瓷瓶可以盛装氢氟酸。
参考答案:B
本题解析:略
本题难度:一般