1��ѡ���� �����й��Ȼ�ѧ����ʽ��������ȷ���ǣ�������
A����101Kpaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8KJ����������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g��=2H2O��l����H=+285.8KJ/mol
B��CO��g����ȼ������283.0kJ/mol����2CO2��g���T2CO��g��+O2��g����Ӧ�ġ�H=2��283.0kJ/mol
C����ϡ��Һ��H+��aq��+OH-��aq��=H2O��l����H=-57.2?kJ/mol?������0.5?mol?H2SO4��Ũ�����뺬1?mol?NaOH��ϡ��Һ��ϣ��ų�����������57.2?kJ
D����֪2H2��g��+O2��g��=2H2O��l����H1��2H2��g��+O2��g��=2H2O��g����H2�����H1����H2
�ο��𰸣�B
���������
�����Ѷȣ�һ��
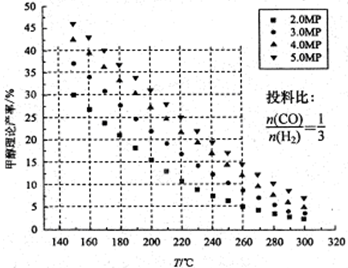
2������� CO2�Ĺ̶��������ڽ������������ŷ��о�����Ҫ���ã���CO2����ϳɼ״�����������Ч�������ѹ�����������ۺ����õ�һ����;����CO2��H2�ڴ����������ܷ�����ӦCO2��3H2 CH3OH��H2O����ü״������۲����뷴Ӧ�¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ����ش��������⣺
CH3OH��H2O����ü״������۲����뷴Ӧ�¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ����ش��������⣺
��1����״����ʵĴ�ʩ�� ��
��2������ͼ�����ݿ�֪����220 �桢5MPaʱ��CO2��ת����Ϊ ���ٽ��¶Ƚ�����
140�棬ѹǿ��С��2MPa����ѧ��Ӧ���ʽ� �������С �� ���䡰 ��ͬ����CO2��ת���ʽ� ��
��3��200��ʱ����0.100molCO2��0.275molH2����1L�ܱ������У��ڴ��������·�Ӧ�ﵽƽ�⡣��CO2��ת����Ϊ25%������¶��¸÷�Ӧ��ƽ�ⳣ��K�� ��(Ҫ��д����ʽ�ͼ�����)
��4����֪��֪��CO��ȼ���ȡ�H����283.0KJ/mol��2H2(g)+O2(g)��2H2O(g) ��H����483.6KJ/mol��
CO(g)+2H2(g)��CH3OH(g) ��H����90.1KJ/mol��д��CO2��H2�ϳɼ״����Ȼ�ѧ����ʽ ��
�ο��𰸣���1�����¡���ѹ��2�֣� ��2��25%��2�֣� ��С��2�֣� ����2�֣�
��3�� ��
��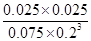 ��1.04 ��3�֣�
��1.04 ��3�֣�
��4��CO2(g)��3H2(g)===CH3OH(g)��H2O(g) ?H��-48.9 kJ/mol��3�֣�
�����������1������ͼ���֪�������¶ȵ����ߣ��״��IJ��ʽ��ͣ���˵������Ӧ�Ƿ��ȷ�Ӧ�����¶���ͬʱ������ѹǿ���״��IJ�������������״����ʵĴ�ʩ�ǽ��¡���ѹ��
��2������ͼ�����ݿ�֪����220 �桢5MPaʱ���״��IJ�����25%������̼ԭ���غ㣬1molCO2����1mol�״�����˼״��IJ��ʾ���CO2��ת���ʣ�����CO2��ת����Ϊ25%�����²�ͬʱ����ѹǿ����Ӧ���ʼ�С����������Ӧ�Ƿ��ȵ������С�Ŀ��淴Ӧ����˽��ºͽ���ѹǿƽ���������Ӧ�����ƶ�������CO2��ת��������
��3�� CO2(g)��3H2(g)===CH3OH(g)��H2O(g)
��ʼŨ�ȣ�mol/L��0.100 0.275 0 0
ת��Ũ�ȣ�mol/L��0.0250 0.0750 0.0250 0.0250
ƽ��Ũ�ȣ�mol/L��0.0750 0.200 0.0250 0.0250
���Ը��¶��·�Ӧ��ƽ�ⳣ��K�� ��
��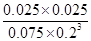 ��1.04
��1.04
��4��CO��ȼ���ȡ�H����283.0KJ/mol�������Ȼ�ѧ����ʽ��2CO(g)��O2(g)��2CO2(g) ��H����566.0KJ/mol������Ϊ��Ӧ��2H2(g)+O2(g)��2H2O(g) ��H����483.6KJ/mol����CO(g)+2H2(g)��CH3OH(g) ��H����90.1KJ/mol�����Ը��ݸ�˹���ɿ�֪��(�ۡ�2���٣���)��2�����õ���ӦCO2(g)��3H2(g)===CH3OH(g)��H2O(g)�����Ը÷�Ӧ�ķ�Ӧ��?H������90.1KJ/mol��2��566.0KJ/mol��483.6KJ/mol����2��-48.9 kJ/mol��
���㣺���鿼����������Է�Ӧ���ʺ�ƽ��״̬��Ӱ�죻��Ӧ���ʺ�ƽ�ⳣ���ļ����Լ���˹���ɵ�Ӧ��
�����Ѷȣ�����
3�������� ��֪��2H2 ( g ) + O2 ( g ) = 2H2O ( l ); ��H = ��571.6kJ/mol
2H2 ( g ) + O2 ( g ) = 2H2O ( g ); ��H = ��483.6kJ/mol
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ); ��H = ��890 kJ/mol
��״���£�ȡ����������Ļ������11.2 L��ȫȼ�պ�ָ������£���ų�������Ϊ203.32kJ�������������м������������ȡ�
�ο��𰸣�V(CH4)
���������
�����Ѷȣ�һ��
4������� �����ŷ�CO2����ɡ�����ЧӦ������ѧ�������о���ν�CO2ת��Ϊ�����õ���Դ������һ�ַ������ǽ�CO2ת��Ϊ������ȼ�ϼ״���CH3OH�����仯ѧ����ʽΪ��

����գ�
��1��д��������Ӧ��ƽ�ⳣ������ʽ______��
��2�����ݻ�Ϊ2L���ܱ������У���һ�����Ķ�����̼��һ����������һ�������ºϳɼ״���ʵ������ͼ��ʾ������˵����ȷ����______������ţ�
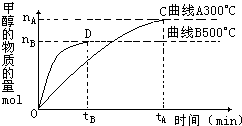
A����300�棬�ӷ�Ӧ��ʼ��ƽ�⣬�״���ƽ����Ӧ����v��CH3OH��=
mol?��L?min��-1
B����Ӧ��ϵ��300�����µ�500�棬ƽ�ⳣ��K�仯��
C���÷�Ӧ������ӦΪ���ȷ�Ӧ
D������C��ķ�Ӧ��ϵ��300�����ߵ�500�棬����
��3��25�棬1.01��105Paʱ��16g?Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�369.2kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ��______��
��4��ѡ�ú��ʵĺϽ�Ϊ�缫�����������ơ��״���ˮ������Ϊԭ�ϣ������Ƴ�һ���Լ״�Ϊԭ�ϵ�ȼ�ϵ�أ��˵�صĸ���Ӧ�����ͨ���������______�������ĵ缫��Ӧʽ��______��
�ο��𰸣���1������K=�������Ũ����֮�����Է�Ӧ���Ũ����֮�����ó�K=c(CH3OH)?c(H2O)c(CO2)?c3(H2)���ʴ�Ϊ��K=c(CH3OH)?c(H2O)c(CO2)?c3(H2)��
��2��A����ѧ��Ӧ���ʵ��ڵ�λʱ��������Ũ�ȵı仯�����״���ƽ����Ӧ����v��CH3OH��=nA2tAmol?��L?min��-1����A����
B������ͼʾ��Ϣ�������¶ȣ��״������ʵ������٣����Է�Ӧ������У�����Ӧ�Ƿ��ȷ�Ӧ�����ڷ��ȷ�Ӧ�������¶ȣ�ƽ�ⳣ����С����B����
C������ͼʾ��Ϣ�������¶ȣ��״������ʵ������٣����Է�Ӧ������У�����Ӧ�Ƿ��ȷ�Ӧ����C��ȷ��
D��C��ʱ��Ӧ�ﵽƽ��״̬�������¶ȣ����ڸ÷��ȷ�Ӧ��ƽ��������У�����n(H2)n(CH3OH)����D��ȷ��
��ѡCD��
��3��16g?Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�369.2kJ����������1mol?Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�725.8kJ�����������Ȼ�ѧ����ʽΪ��
CH3OH��l��+32?O2=CO2��g��+2H2O��l����H=-725.8kJ/mol���ʴ�Ϊ��CH3OH��l��+32?O2=CO2��g��+2H2O��l����H=-725.8kJ/mol��
��4���״�Ϊԭ�ϵ�ȼ�ϵ���У�ȼ�ϼ״�Ϊ����������ʧ���ӵ�������Ӧ�������������������õ��ӵû�ԭ��Ӧ�����������Լ���ֻ��ѡ����������Ϊ����ʣ��ڼ��Ի����£������ķŵ����Ϊ��O2+2H2O+4e-=4OH-���ʴ�Ϊ���״���O2+2H2O+4e-=4OH-��
���������
�����Ѷȣ�һ��
5������� ��1����֪��C3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) ��H=��2220.0kJ/mol
H2O(1) ===H2O(g)����H=+44.0kJ/mol
д������ȼ������CO2����̬ˮ���Ȼ�ѧ����ʽ ��
��2������ͼ��ʾ��ʵ��װ���У�EΪһ���õ��۵⻯����Һ��ʪ����ֽ��C��DΪ������ֽ���˵IJ��У�X��Y�ֱ�Ϊֱ����Դ����������A��B�г���AgNO3��Һ������ʢ��AgNO3��Һ��ˮ���У��ٷֱ���벬�缫���жϵ�Դ����S1���պϿ���S2��ֱͨ����һ��ʱ���B�缫�������أ�A��������ɫ���塣��ش��������⣺
�� д��D�缫��Ӧʽ���������������� ��
��д��ˮ���е��AgNO3��Һ�ܷ�Ӧ�����ӷ���ʽ�� ����������2.16 g���������Ϸų��������ڱ�״���µ������____ _L��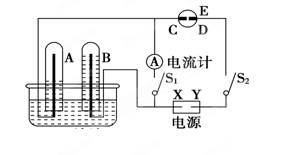
�ο��𰸣���1��C3H8(g)��5O2(g)��3CO2(g)��4H2O(g) ��H����2044kJ/mol��3�֣�
��2��2I����2e����I2(2��)��4Ag����2H2O 4Ag��4H����O2��(2��)��0.112(2��)
4Ag��4H����O2��(2��)��0.112(2��)
�����������1����֪����C3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) ��H����2220.0kJ/mol����H2O(1) ===H2O(g)����H��+44.0kJ/mol������ݸ�˹���ɿ�֪��+�ڡ�4���õ�����ȼ������CO2����̬ˮ���Ȼ�ѧ����ʽC3H8(g)��5O2(g)��3CO2(g)��4H2O(g)�����Ը÷�Ӧ�ķ�Ӧ�ȡ�H����2220.0kJ/mol+44.0kJ/mol��4����2044kJ/mol��
��2�����жϵ�Դ����S1���պϿ���S2���ɵ��ء�ֱͨ����һ��ʱ���B�缫�������أ���˵��B�缫����������Һ�еĽ��������ӷŵ�����������A������������Һ�е�OH���ŵ������ɫ��������������Y�缫�ǵ�Դ�ĸ�����X����������D�缫����������Һ�еĵ����ӷŵ����ɵ��ʵ⣬�缫��ӦʽΪ2I����2e����I2��
�ڶ��Ե缫�����������Һ�������ᡢ�������������ӷ���ʽΪ4Ag����2H2O 4Ag��4H����O2������������2.16 g��������������2.16g�����ʵ�����2.16g��108g/mol��0.02mol�����Ը��ݷ���ʽ��֪���������������ʵ�����0.02mol��4��0.005mol������ڱ�״���µ������0.005mol��22.4L/mol��0.112L��
4Ag��4H����O2������������2.16 g��������������2.16g�����ʵ�����2.16g��108g/mol��0.02mol�����Ը��ݷ���ʽ��֪���������������ʵ�����0.02mol��4��0.005mol������ڱ�״���µ������0.005mol��22.4L/mol��0.112L��
���㣺�����˹���ɵ�Ӧ�á��绯ѧԭ����Ӧ�á��ж������
�����Ѷȣ�����