1��ʵ���� ��15�֣�Ϊ��̽��H2O2��H2SO3��Br2�����Ե����ǿ�����������ʵ�飨�г���������ȥ������ش��������⣺
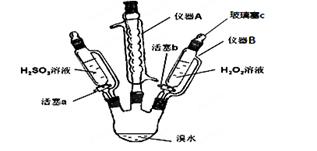
��1������A������_________����������___________��
��2��������B�μ�Һ�岢����Ҫ������c��ԭ����____________________________��
��3��ʵ���¼���£��벹ȫ�հף���
����
| ʵ�����
| ʵ������
| ʵ�����
|
��
| ����a����μ���H2SO3��Һ������
| ________________
| __________________________
|
��
| �����������Һ����μ���H2O2��Һ
| �տ�ʼ��Һ��ɫ�����Ա仯�������μӣ���Һ��Ϊ�Ȼ�ɫ
| __________________________
|
��4��������У���ʼʱ��ɫ�����Ա仯��ԭ���ǣ�д��һ����_______________________��
������з�Ӧ�����ӷ���ʽ_________________________________________________��
���������Ҫ��Ӧ�����ӷ���ʽ_____________________________________________��
2��ѡ���� �ж��������ʵ�����������ǿ������˳����
[? ]
A��FeCl3>C12>I2
B��C12>I2>FeCl3
C��I2>Cl2>FeCl3
D��C12>FeCl3>l2
3��ѡ���� ����ͬ�����µ�������Ӧ��
��2A-+B2=2B-+A2
��2C-+A2=2A-+C2
��2B-+D2=2D-+B2
�ɴ˵ó��������жϲ���ȷ���ǣ�������
A�������ԣ�D2��B2��A2��C2
B��2A-+D2�T2D-+A2�÷�Ӧ�ܽ���
C����ԭ�ԣ�C-��A-��B-��D-
D��2B-+C2�T2C-+B2�÷�Ӧ�ܽ���
4��ѡ���� �����£���H2O2��Һ�еμ�����FeSO4��Һ���ɷ�������������Ӧ��2Fe2++H2O2+2H+=2Fe3+ +2H2O
2Fe3+ +H2O2 =2Fe2+ +O2��+2H+ ����˵����ȷ����
[? ]
A��H2O2�������Ա�Fe3+ǿ���仹ԭ�Ա�Fe2+��
B����H2O2�ֽ�����У���Һ��pH���½�
C����H2O2�ֽ�����У�Fe2+��Fe3+���������ֲ���
D��H2O2��������Ҫ�ϸ�������Fe2+
5��ѡ���� ���ݷ�Ӧʽ����2Fe3++2I-=2Fe2++I2 ��2Fe2++Br2=2Fe3++2Br-�����ж����ӵĻ�ԭ�Դ�ǿ������˳����
[? ]
A��Br-��Fe2+��I-
B��I-��Fe2+��Br-
C��Br-��I-��Fe2+
D��Fe2+��I-��Br-