1、填空题 2007年诺贝尔化学奖授予德国化学家格哈德・埃特尔,以表彰他在“固体表面的化学过程”研究中取得的杰出成就。不同物质接触面的过渡区称为界面,若其中一物质为气态时,这种界面通常称为表面;在其表面上所发生的一切物理化学现象统称为表面现象,而研究各种表面现象实质的科学称为表面化学。
(1)下列哪些研究属于表面化学研究的范畴?____________(填写字母代号)。
A.钢铁的生锈
B.以铁的氧化物为催化剂合成氨
C.以铂、铑等为催化剂,将汽车尾气中的氮的氧化物与CO等转化为无污染物质
D.用惰性材料为电极,组成甲烷-空气燃料电池将化学能转化成电能
(2)列举硫酸工业中属于“表面化学”范畴的中学化学反应,写出化学方程式:__________________________________。
(3)化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如下图所示,(注:图中ΔE都为正值)
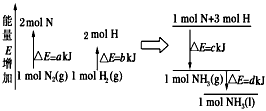
写出该反应的热化学方程式:__________________________________。
(4)合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3,当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化剂活性最高,以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉。发生如下反应:2Fe2O3+C 4FeO+CO2,为制得该种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为____________g。
4FeO+CO2,为制得该种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为____________g。
2、选择题 三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热△H?=?-3677kJ/mol(磷元素被氧化为P4O10),下列有关P4S3的说法中不正确的是?
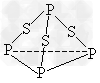
[? ]
A.分子中每个原子最外层均达到8电子稳定结构
B.P4S3中磷元素为+3价
C.热化学方程式为P4S3(?s)+8O2(g)=P4O10(s?)+3SO2(g);△H?=-3?677kJ/mol
D.分子中存在极性键与非极性键
3、填空题 (14分)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法Ⅰ
| 用炭粉在高温条件下还原CuO
|
方法Ⅱ
| 电解法:2Cu+H2O 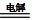 Cu2O+H2↑ Cu2O+H2↑
|
方法Ⅲ
| 用肼(N2H4)还原新制Cu(OH)2
|
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成 而使Cu2O产率降低。
(2)已知:①C(s)+O2(g)=CO2(g) △H=akJ・mol―1;
②2CO(g)+O2(g)=2CO2(g) △H=bkJ・mol―1;
③2Cu2O(s)+O2(g)=4CuO(s) △H=ckJ・mol―1.
方法Ⅰ制备过程会产生有毒气体,写出制备反应的热化学方程式 。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为 。
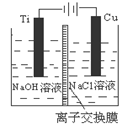
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为 。
(5)方法Ⅲ可以用甲醛稀溶液替代肼,但因反应温度较高而使部分产品颗粒过大, (填操作名称)可分离出颗粒过大的Cu2O。
(6)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:
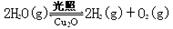
4、填空题 (3分)发射卫星用 作燃料,
作燃料, 作氧化剂,两者反应生成N2和水蒸气,已知:
作氧化剂,两者反应生成N2和水蒸气,已知:
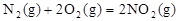 △H1=+67.7kJ/mol
△H1=+67.7kJ/mol
N2H4(g)+O2(g)= N2(g)+2H2O(g) △H2=-534kJ/mol
试写出N2H4与 NO2反应的热化学方程式
。
5、简答题 水是宝贵资源,研究生活和工业用水的处理有重要意义.

请回答下列问题:
(1)已知水的电离平衡曲线如图1所示.A、B、C三点水的电离平衡常数KA、KB、KC关系为______,若从B点到D点,可采用的措施是______(填序号).
a.加入少量盐酸
b.加入少量碳酸钠
c.加入少量氢氧化钠
d.降低温度
(2)饮用水中的NO3-主要来自于NH4+.已知在微生物的作用下,NH4+经过两步反应被氧化成NO3-.两步反应的能量变化如图2,1molNH4+全部被氧化成NO3-的热化学方程式为______.
(3)某工厂用电解法除去废水中含有的Cr2O72-,总反应方程式为:Cr2O72-+6Fe+17H2O+2H+?2Cr(OH)3↓+6Fe(OH)3↓+6H2↑,该电解反应的负极材料反应的电极式为______,若有9mol电子发生转移,则生成的cr(OH)3物质的量为______.
(4)废水中的N、P元素是造成水体富营养化的主要因素,农药厂排放的废水中.常含有较多的NH4+和PO43-,其中一种方法是:在废水中加入镁矿工业废水,可以生成高品位的磷矿石--鸟粪石,反应的离子方程式为Mg2++NH4++PO43-→MgNH4PO4↓.该方法中需要控制污水的pH为7.5-10,若pH高于l0.7,鸟粪石产量会降低,其原因可能是______.