| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《热化学方程式》试题强化练习(2019年最新版)(一)
 2、填空题 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
试判断K1 K2(填写“>” “ =”或“<”)。 (2)用2mol N2和3mol H2合成氨,三容器的反应温度分别为T1、T2、T3且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时N2的质量分数如图所示,此时甲、乙、丙三个容器中一定达到化学平衡状态的是 ,都达到平衡状态时,N2转化率最低的是 。 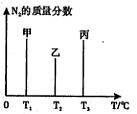 (3)NH3与CO2在120oC,催化剂作用下可以合成反应生成尿素:CO2 +2NH3  (NH2)2CO +H2O (NH2)2CO +H2O在密闭反应容器中,混合气体中NH3的含量变化关系如图所示  (该条件下尿素为固体)。则A点的正反应/速率  (CO2) B点的逆反应速率 (CO2) B点的逆反应速率 (CO2)(填写“>”“=”或“<”),NH3的平衡转化率为____ ; (CO2)(填写“>”“=”或“<”),NH3的平衡转化率为____ ;(4)已知下列热化学方程式: 2H2(g)+O2(g)=2H2O(1) △H = -571.6kJ/mol N2(g)+O2(g)  2NO(g) △H =+180kJ/mol 2NO(g) △H =+180kJ/mol请写出用NH3还原NO的热化学方程式_ ; (5)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式____ 。科学家利用此原理,设计成氨气-氧气燃料电池,则通人氨气的电极是 (填“正极”或“负极”),在碱性条件下,通人氨气的电极发生的电极反应式为 。 3、选择题 已知在298K时下述反应的有关数据 4、填空题 (13分)碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。 5、填空题 Ⅰ.沿海地区有着丰富的海水资源,海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。合理利用资源和保护环境是可持续发展的重要保证。
(3)火力发电在我国的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:  ①天然海水的pH≈8,试用离子方程式解释天然海水呈弱碱性的原因 (任写一个)。 ②某研究小组为探究提高含硫烟气中SO2吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示。 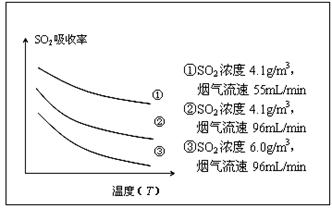 请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议: 。 ③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,使用氧气将其氧化的化学原理是 (任写一个化学方程式或离子方程式)。氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是 。 Ⅱ.能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式 ①2H2(g)+O2(g)=2H2O(l)  H=-570kJ/mol; H=-570kJ/mol;②H2(g)+1/2O2(g)=H2O(g)  H=-242kJ/mol; H=-242kJ/mol;③C(s)+1/2O2(g)=CO(g)  H=―110.5kJ/moL; H=―110.5kJ/moL;④C(s)+O2(g)=CO2(g)  H=―393.5kJ/moL; H=―393.5kJ/moL;⑤CO2(g)+2H2O(g)=2CH4(g)+2 O2(g)  H=+890kJ/moL H=+890kJ/moL回答下列问题 (1)上述反应中属于吸热反应的是 。 (2)H2的燃烧热为△H= 。 (3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s) + H2O(g)=H2(g)+ CO(g)  H=akJ/moL;则a= ;该反应的熵 H=akJ/moL;则a= ;该反应的熵 S 0(选填“>”、“=”、“<”);已知自由能 S 0(选填“>”、“=”、“<”);已知自由能 G= G= H―T H―T S,当 S,当 G<0时可自发进行。则该反应在什么条件下可自发进行__________________。 G<0时可自发进行。则该反应在什么条件下可自发进行__________________。(4)CO分析仪以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是 。 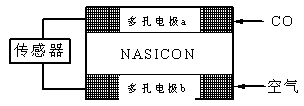 A.负极的电极反应式为:CO+O2― |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《原电池原理》高频.. | |