1�������� ��8�֣��ڼ��������£���MnO2������Ũ���ᷴ Ӧ���Ƶ�����0.56L����״�������ʣ�
Ӧ���Ƶ�����0.56L����״�������ʣ�
��1����������Ҫ����MnO2���ٿˣ�
��2����������HCl�����ʵ����Ƕ��٣�
�ο��𰸣���1�����MnO2?2.18g?��4�֣���2����������HCl�����ʵ�����0.05mol����6�֣�
�����������
�����Ѷȣ�һ��
2��ѡ���� ����ʱ��2011��3��11��13ʱ46�֣��ձ����ݵ���̨���Զ�130 km������9.0��ǿ�ҵ��𣬲����������ģ��Х���ڿ��������Ҫ�ô���Ư�ۺ�Ư��Һ�����ֵ�������ɱ�����������й���Ư�ۺ�Ư��Һ˵������ȷ����
A��Ư���Ǵ����Ư��Һ�ǻ����
B��Ư�۵���Ч�ɷ���Ca(ClO)2
C����ҵ�Ͻ�����ͨ�����ʯ��ˮ��ȡƯ��
D��Ư��Һ����Ч�ɷ���Na2O2
�ο��𰸣�B
���������A��Ư�۵���Ҫ�ɷ���CaCl2��Ca(ClO)2���ǻ�������B��Ư�۵���Ч�ɷ���Ca(ClO)2����ȷ��C����ҵ�Ͻ�����ͨ���������Ƶ�����Һ����ȡƯ�ۣ�����D��Ư��Һ����Ч�ɷ���Ca(ClO)2������
�����Ѷȣ�һ��
3��ѡ���� ���й�����������ˮ��˵������ȷ���ǣ�������
A���ڼ�ѹ����������ת��ΪҺ�ȣ����ø���ĸ�ƿ����Һ��
B���������������ʹ�������ɫ������ɫ
C��������ˮ�ڹ����������������ݳ������������Ҫ�ɷ���O2
D��������ˮ����ʹ��ɫʯ����ֽ�ȱ�����ɫ
�ο��𰸣�A��Һ�������ĸ�ƿ����Ӧ�����Կ��ø���ĸ�ƿ����Һ�ȣ���A��ȷ��
B��������������߱�Ư���ԣ�������Ư�����õ��Ǵ����ᣬ���Ը������������ʹ�������ɫ������ɫ����B����
C��������ˮ������Ӧ��Cl2+H2O�TH++Cl-+HClO��HClO���ȶ��������ֽ������������C��ȷ��
D��������ˮ������Ӧ��Cl2+H2O�TH++Cl-+HClO��H+������ʹ��ɫʯ����ֽ��죬HClO����Ư���ԣ�ʹ��ֽ��ɫ����D��ȷ��
��ѡ��B��
���������
�����Ѷȣ�һ��
4��ѡ���� ���������У�����ʹ�������ɫ������ɫ���ǣ�?����
A��Cl2
B����ˮ
C��NaClO��Һ
D��HClO
�ο��𰸣�A
�������������û��Ư���ԣ���������ˮ���ɵĴ��������ǿ�����ԣ���ʹ��ɫ������ɫ�������������Ҳ��ʹ��ɫ������ɫ��������ȷ�Ĵ�ѡA��
�����������ǻ���������Ŀ��飬����ע�ػ��������������ѵ�����ѶȲ�������������ѧ������˼ά�����ͷ�ɢ˼ά������
�����Ѷȣ���
5��ʵ���� ʵ����������������ҩƷ��ȡ���﴿����������
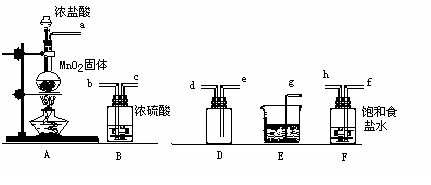
С��1:�����������ң�װ����ȷ������˳��Ϊ��?���ӣ�?���ӣ�?���ӣ�?���ӣ�?���ӣ�?���ӣ�?���ӣ�?��������ӿ���ĸ��
С��2: װ��F��������??��װ��E��������?��
С��3:װ��A��E�еķ�Ӧ��ѧ����ʽΪ :
:
С��4:ijУ��ѧ��ȤС���ȡ8.7g��������������10mol��L��Ũ���ᷴӦ�������Ͽ��Ƶ��������������״����V1 = ??L
С��5:����С����ȡ��10mol/L��Ũ����40ml���������Ķ������̷�Ӧ�������ϲ������������ΪV2����״��������V1?V2�����������������������ԭ����?
�ο��𰸣�
��1:��? a?���� f?���� h?����? b?���� c?����? e?���� d?���� g?��
С��2:?���������л��е��Ȼ���?��?���ն��������?��
С��3: ?A ��MnO2+4HCl(Ũ)
?A ��MnO2+4HCl(Ũ)  ?MnCl2+Cl2��+2H2O? E�� Cl2+2NaOH=NaCl+NaClO+H2O ��
?MnCl2+Cl2��+2H2O? E�� Cl2+2NaOH=NaCl+NaClO+H2O ��
��4:2.24 L
С��5:��?ԭ�������ŷ�Ӧ���У�����Ũ�ȼ�С��ϡ�����������̷�Ӧ
���������ʵ������ȡ������ҩƷ��Ũ����Ͷ������̣�����Ũ������лӷ��ԣ����������л�����Ȼ��⣬�������ռ�֮ǰ��Ҫ��ȥ�Ȼ��⣬���ñ���ʳ��ˮ�����Ȼ��⡣��Ϊ��Ҫ�������������˻�Ҫͨ��Ũ������и��Ȼ������ռ�����Ϊ�������ܶȴ��ڿ����ģ����Կ�ͨ�����������������ռ��������ж��������Ҫ����β���������Է�ֹ��Ⱦ���������ն��ڵ�������������������Һ�����ݷ�ӦMnO2+4HCl(Ũ)  ?MnCl2+Cl2��+2H2O��֪��ÿ����87g�������̣��Ϳ�������22.4L��״���µ�����������8.7g�������̿�����2.24L������40ml 10mol/L��Ũ��������ʵ�����0.4mol�����ݷ�Ӧʽ��֪������Ӧ������0.1mol�������������ڷ�Ӧ�����������Ũ�����ͣ������͵�һ���̶�ʱ���������̾Ͳ������������ᣬ����ʵ�����ɵ��������ҪС��0.1mol��
?MnCl2+Cl2��+2H2O��֪��ÿ����87g�������̣��Ϳ�������22.4L��״���µ�����������8.7g�������̿�����2.24L������40ml 10mol/L��Ũ��������ʵ�����0.4mol�����ݷ�Ӧʽ��֪������Ӧ������0.1mol�������������ڷ�Ӧ�����������Ũ�����ͣ������͵�һ���̶�ʱ���������̾Ͳ������������ᣬ����ʵ�����ɵ��������ҪС��0.1mol��
�����Ѷȣ�һ��