|
|
|
高考化学试题《水的电离平衡》考点巩固(2019年最新版)(一)
2020-07-28 03:46:22
【 大 中 小】
|
1、填空题 下列物质中,属于电解质的是______(填序号),写出任意电解质在水溶液中的电离方程式______
A.氯化钠溶液?B.硫酸?C.醋酸?D.氯化银?E.酒精?F.蔗糖?G.氨气
H.三氧化硫?I.铜?J.硫酸钡.
2、选择题 向稀硫酸溶液中逐渐加入氨水,当溶液中c(NH4+)=2c(SO42-)时,溶液的pH ( )
A.等于7
B.大于7
C.小于7
D.无法判断
|
3、填空题 已知水在25?℃和95?℃时,其电离平衡曲线如图所示
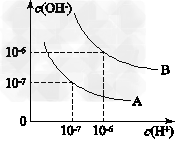
(1)则25?℃时水的电离平衡曲线应为________(填“A”或“B”),请说明理由_________________________________________________。
(2)25?℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为________。
(3)95?℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,pH1与pH2之间应满足的关系是________。
(4)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。请分析其原因___________________________。
4、选择题 常温下,用0.1000mol/LNaOH溶液分别滴定25.00mL0.1000mol/L盐酸溶液和
25.00mL0.1000mol/LCH3COOH溶液,滴定过程中pH变化曲线如下图所示。下列判断不正确的是
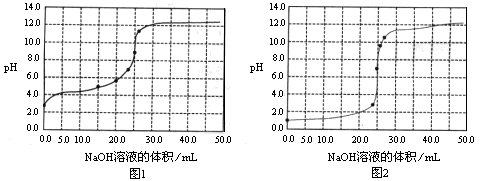
A.滴定盐酸的pH变化曲线为图2
B.在滴定CH3COOH溶液的过程中,始终都有c(Na+)+ c(H+)=c(CH3COO
|
5、选择题 已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol/L的一元酸HA与b mol/L一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.混合溶液的pH=7
B.混合溶液中,c(H+)= mol/L
mol/L
C.a=b
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
 mol/L
mol/L