1��ʵ���� ��������(CaO2)������������������ҩ�����졢?��֬Ư����������������������Ϊ�������������SO2ͨ��������ƹ����ĩ��������?���ɡ����������CO2��SO2�������?�Ƶķ�Ӧԭ����ͬ����Ҳ���������SO2���н�ǿ�Ļ�ԭ�ԣ�CO2��ǿ��ԭ�ԣ���Ӧԭ������ͬ���ݴ��������ʵ����������ж�?��
ʵ��һ��ͨ����������IJ����жϷ����Ļ�ѧ��Ӧ��ʵ��װ�����£�?
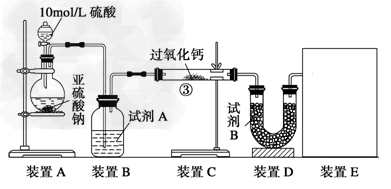
(1)�Լ�A����ѡ��____________���Լ�BΪ��ʯ����������______________________��
(2)װ��E���ڲⶨ����?�����?�����ڿ��л���װ��ͼ��
(3)ʵ����װ?��C����m1?g��װ��D����m2?g��װ��E���ռ���V?L����(�ѻ���ɱ�״����)���������йز��������жϣ���SO2δ����ʱ��V��m1��m2�Ĺ�ϵʽΪ_________����SO2��ȫ������д����Ӧ�Ļ�ѧ����ʽ��__________________________��
ʵ�������һ�����Ĺ������ƹ�����ͨ������SO2��ȡ��Ӧ��Ĺ������ʵ��̽������֤������������SO2��Ӧ���ص㡣������裺
����1����Ӧ�������ֻ��Na2SO3��SO2δ������
����2����Ӧ�������ֻ��Na2SO4��SO2��ȫ������
����3?��________________________��
ʵ��̽����
(4)���ʵ��֤������3����ȷ�ģ���Ҫ�ش�ʵ����̡�����ͽ��ۣ�________________ ________________________________��
ʵ?�����ۣ�
(5)ʵ�������SO2��ͨ����ֱ��Ӱ��̽��ʵ�����Ŀ�ѧ�ԣ����Ҫ˵��ԭ�� _______________________________________��?
�ο��𰸣�(1)Ũ���� ������δ��Ӧ��SO2
(2)? (���������𰸾���)
(���������𰸾���)
(3)?V��7m1/30������CaO2��SO2===CaSO4? ����Ӧ�����ΪNa2SO3��Na2SO4�Ļ���SO2��������
(4)ȡ������Ӧ��Ĺ�������Թ��У�������ˮ�ܽ⣬����BaCl2��Һ�а�ɫ�����������ټ���ϡ���ᣬ���������ܽ⣬֤��ԭ�����м�����������Ҳ�������ƣ���Na2O2��SO2����������
(5)��Na2O2ʣ�࣬�����ˮ�ܽ⣬���������ܽ�SO32��������SO42����
���������
�����Ѷȣ�һ��
2��ѡ���� ����ʵ�������ԭ������ȷ����(? )

A����ȥ�Ȼ��ƾ����������������
B��ֽ�������е�չ����֮�����ܹ�չ������Ҫԭ����ëϸ����
C��ֻ�õ�����Һ���ɼ���ӵ�ʳ�����Ƿ����Σ��ӵ�ˮ����ȡ���ʵ�ʱ����������ˮ�Ҵ�����CCl4
D���������Ƶ�Cu��OH��2����Һ���������д��ڵĸ���
�ο��𰸣�C
�����������
�����Ѷȣ���
3��ʵ���� ij�о���ѧϰС�����ʵ�鷽�����о�ϡ������ͭ��Ӧ����NO��

��1�������������ʵ�鲽�裺
��_____________��
�ڴ���A����U���Ҳ�©����ע��ϡ���ᣬһֱע��ϡHNO3�Ӵ���A����Ƥ��Ϊֹ�� �۹رջ���A���۲�ʵ������
��2����¼�����۲쵽��ʵ�����ɹ۲쵽�������У�U�����ͭ˿���ܽ⣬��__________ɫ�����������Һ����ɫ�����ŷ�Ӧ���Ͻ��У����Ӧ����ֹͣ���ù��̷�Ӧ�����ӷ���ʽΪ_____________��
��3��Ϊ�˽�һ��֤����Ӧȷʵ���ɵ�NO������Ҫ�IJ���������������Ϊ____________��
��4����2.56?g?ͭ����100mLϡ���ᷴӦ����ַ�Ӧ���ռ�����״����NO���Ϊ1.12L�������Һ��ʣ��NO3-�����ʵ���Ũ��Ϊ1.0mol/L����ԭϡ��������ʵ���Ũ��__________?(��Һ����仯���Բ���)��
�ο��𰸣���1�����װ��������
��2����?��?3Cu+8H++2NO3-=3Cu2+ +2NO +4H2O
+4H2O
��3������A���к���ɫ�������
��4��1.5?mol/L
���������
�����Ѷȣ�һ��
4������� ����ѧ����ŵʵ�顱�����û�ѧ��Ӧ�����������ѹ����ʹ�����ѧ��Ӧ���η�������ͼ��ʾ����һ������ѧ����ŵʵ�顱������A��Fװ���зֱ�ʢ�ŵ�����Ϊ��A��ϡ���B��п����C��ij��Һ��D��CaCO3���壻E��������ɫʯ����Һ������ˮ��F�������ij���ʯ��ˮ��ش��������⣺
��1����Ӧ��ʼ����E�г��ֺ�ɫ��F���а�ɫ�������ɣ���C�е����ʿ�����______��
��2��װ��D�е����ӷ���ʽ______���÷�Ӧ��������______��װ��F�е����ӷ���ʽ______��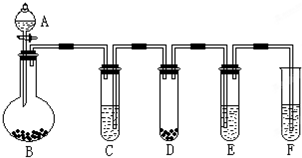
�ο��𰸣�����ѧ����ŵʵ�顱�����÷�Ӧ�����������ѹ���ͺ�������ԭ����ʹ���ɻ�ѧʵ�����η�������������ֻ��Ҫ���Ƶ�һ����Ӧ��
��1��Ӧ��ʼ����E�е�����ɫʯ����Һ������ˮ���ֺ�ɫ��˵���������������ɣ�F�������ij���ʯ��ˮ�а�ɫ�������ɣ��������Ϊ������̼���������ȣ���ΪD����̼��ƹ��壬F���dz���ʯ��ˮ�����Ը�����ֻ���Ƕ�����̼��ϡ�����ϡ���ᶼ�ɺ�̼��Ʒ�Ӧ���ɶ�����̼������C�е����ʿ�����ϡ�����ϡ���ᣬ
�ʴ�Ϊ��ϡ�����ϡ���
��2��̼��ƺ��ᷴӦ���ɸ����ӡ�ˮ�Ͷ�����̼��̼��ơ�ˮ�Ͷ�����̼д��ѧʽ������װ��D�е����ӷ���ʽ���ӷ���ʽΪ��CaCO3+2H+�TCa2++H2O+CO2�����÷�Ӧ������η�Ӧ�������������Σ������Ǹ��ֽⷴӦ��������̼ʹ�����ʯ��ˮ����ǣ�������̼���������Ʒ�Ӧ����̼��ƺ�ˮ������װ��F�з�Ӧ�����ӷ���ʽΪCO2+Ca2++2OH-�TCaCO3��+H2O
�ʴ�Ϊ��CaCO3+2H+�TCa2++H2O+CO2�������ֽⷴӦ��CO2+Ca2++2OH-�TCaCO3��+H2O��
���������
�����Ѷȣ�һ��
5��ѡ���� �ñ�Ũ�ȵ�����ζ�δ֪Ũ�ȵ�NaOH��Һ�����и�����������������ȷ���л���ɲⶨ���ƫ�͵���
A����ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ
B���ζ��յ����ʱ���Ӷ���
C��������ˮϴ����ʽ�ζ��ܺ�װ���������еζ�
D����ƿˮϴ��δ����
�ο��𰸣�B
�����������
�����Ѷȣ���