1������� ijͬѧ��ľ̿��Ũ���ᷴӦ���о�Ũ��������ʣ�����������
��ľ̿��Ũ���ᷴӦ�Ļ�ѧ����ʽ��______��
�ڸ�ʵ��۲쵽
a�����Ը��������Һ��ɫ��dz?
b������ʯ��ˮ�����
�ܹ�֤��Ũ������������Ե�ʵ��������______������ĸ����
�����Ը��������Һ��������______��
����ľ̿��Ũ���ᷴӦ�����������������Ϊ0.64g����Ӧת�Ƶ��ӵ����ʵ���Ϊ______��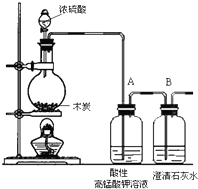
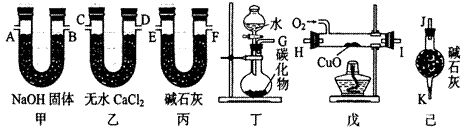
2������� ��16�֣�ij��ѧ��ȤС��ͬѧ�������и�����װ����ȡ��ϩ�����ù�����������C2H4������CO2��H2O���ⶨ�� ϩ��̼��������Ԫ�ص������ȡ�
ϩ��̼��������Ԫ�ص������ȡ�
�ش��������⣺
��1����ͬѧ��ʵ�����Ʊ�C2H2�����������CaC2��ZnC2��Al4C3��Mg2C2��Li2C2��ѡ��һ���Լ���ˮ��Ӧ���Ʊ���ϩ��д���÷�Ӧ�Ļ�ѧ ����ʽ��?��
����ʽ��?��
��2��������������������������װ�õ��ܵ�����˳���ǣ�G��E��F��?��?��
?��?��A��B��J��
��3��װ�ü�������?��
װ�ü���������?��
��4��װ������CuO��������?��
��5��ʵ��ǰ�Ƶüס�����װ�õ������ֱ�Ϊm1g��n1g��ʵ����ϣ��Ƶüס�����װ�õ������ֱ��Ϊm2g��n2g������ϩ������̼ԭ�Ӻ���ԭ�ӵ�ԭ�Ӹ�����Ϊ?���г���ʽ����
��6��������û��CuO����ⶨ���?���ƫ�ߡ�����ƫ�͡����䡱����ͬ���������ӱ�װ�ã���ⶨ���? ?��
?��
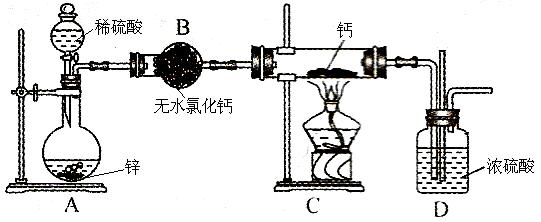
3��ʵ���� ��10�֣��⻯�ƣ�CaH2������HԪ�صĻ��ϼ�Ϊ �C1�ۣ������ǵ�ɽ�˶�Ա���õ���Դ�ṩ�����⻯��Ҫ�ܷⱣ�棬һ���Ӵ���ˮ�ͷ�����Ӧ�����������ƺ��������⻯��ͨ��������������Ƽ�����ȡ����ͼ��ģ����ȡװ�á�
��1���⻯����ˮ��Ӧ�Ļ�ѧ����ʽΪ��__________________��
�÷�Ӧ�����������뻹ԭ��������ʵ���֮��Ϊ��__________________��
��2������ͼʾʵ��װ�ý���ʵ�飬ʵ�鲽�����£����װ�������Ժ�װ��ҩƷ����Һ©��������_____________________���밴��ȷ��˳���������в������ţ���
�ټ��ȷ�Ӧһ��ʱ��?���ռ����岢�����䴿��
�۹رշ�Һ©������?��ֹͣ���ȣ������ȴ
��3��װ��B�������ǣ�_____________________________________��Ϊ��ȷ�Ͻ���װ��C�������Ѿ����Ӧ��B��C֮���ٽ�һװ�ã���װ���м�����Լ��ǣ�_____________��
4��ѡ���� ����ʵ�������ȫ��������
A������KMnO4��O2ʱ��Ϊ��ֹ�Թ����Ѻͽ��ܸ�ʴ���Թܿ���������б���ܿڷ�һ����
B������SO2����ʵ��ʱҪ��ͨ����ڽ��У������SO2һ���ŵ�����
C�������ж�����ʣ�İ���Ҫ��CS2����������������
D������������Һʱ������Ͳ��ȡһ�������Ũ�������������ձ��е�ˮ���ֽ����Ѹ��ת�Ƶ�����ƿ��
5��ʵ���� ��12�֣�����ѧ�α��н���������ʵ�飺��һ���������״��ͭ˿���ھƾ���������ȣ���ͭ˿�����ں�������������ʢ��Լ2 mL�Ҵ����Թ�������� �����Ρ�
������
����������������������ȡ��ȩ������Щ���㣨д�����㣩��
?��
��ij����С��������ͼװ�ý����Ҵ��Ĵ�����ʵ�鲢��ȡ��ȩ��ͼ������̨��װ������ȥ���ֺ��߱�ʾ�齺�� ������д���пհף�
������д���пհף�
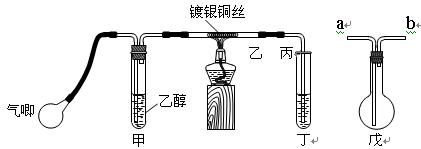
��1����װ�ó�������70��80���ˮԡ�У�Ŀ����?��
��2��ʵ��ʱ���ȼ��Ȳ��������еĶ���ͭ˿��Լ1���Ӻ�����������ʱͭ˿���ʺ���״̬�����Ѿƾ��Ƴ��ߣ�����һ���Ĺ����ٶȣ�ͭ˿�ܳ�ʱ�䱣�ֺ���ֱ��ʵ�������
���Ҵ��Ĵ�������Ӧ��________��Ӧ������ȡ������ȡ������÷�Ӧ�Ļ�ѧ����ʽΪ?��
�ڿ��ƹ����ٶȵķ�����?���������ٶȹ������?���������ٶȹ������?��
��3�����Թܶ�����ˮ���ղ����Ҫ�ڵ����ҡ���֮�������װ�ã������ӷ����ǣ�����װ���е��ܴ��ţ����ҽ�?��_______�ӱ��������ﲻ��ˮ���ն���ֱ����ȴ��Ӧ���Թܶ� ���� _____?�С�
���� _____?��