1、选择题 在反应3BrF3+5H2O====HBrO3+Br2+9HF+O2↑中,若有3 mol水作还原剂时,被水还原的BrF3的物质的量为(?)
A.3 mol
B.2 mol
C. mol
mol
D.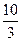 mol
mol
参考答案:B
本题解析:设被水还原的BrF3的物质的量为x。根据电子守恒知:
3 mol×2=x・3
x="2" mol
或根据化学方程式可知,2 mol水可还原 ?mol BrF3,那么,3 mol水还原的BrF3的物质的量为x。则:
?mol BrF3,那么,3 mol水还原的BrF3的物质的量为x。则:
3 mol∶x="2" mol∶ ?mol
?mol
x="2" mol
本题难度:简单
2、填空题 由于NaNO2有毒,将含该物质的废水直接排放会引起水体的严重污染,所以这种废水必须经处理后才能排放。处理方法之一的原理如下:
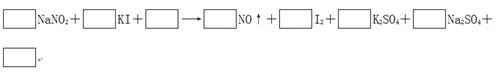 ?
?
(1)请完成并配平该化学方程式。
(2)在上述反应中,若要生成50.8 g I2,则电子转移了________个。
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
________________________________________________________________________。
从环保角度来讲,要处理NaNO2,所用物质的________(填“还原性”或“氧化性”)应该比KI更______(填“强”或“弱”)。
参考答案:(1)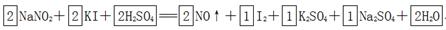
(2)2.408×1023(或0. 4NA)? (3)反应生成了NO,该物质会造成大气污染;还原性;强
本题解析:(1)根据方程式可知,碘化钾中碘元素的化合价从-1价升高到0价,失去1个电子,做还原剂。亚硝酸钠中氮元素的化合价从+3价降低到+2价,得到1个电子,做氧化剂。则根据电子守恒可知氧化剂和和还原剂的物质的量之比时1:1。根据原子守恒可知,反应物中还有硫酸生成,生成物还有水生成,则反应的化学方程式是2NaNO2+2KI+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O。
(2)50.8g单质碘的物质的量是50.8g÷254g/mol=0.2mol,所以转移电子的物质的量是0.2mol×2=0.4mol,个数是0.4NA。
(3)由于反应生成了NO,该物质会造成大气污染,所以该方法不是最佳方法。从环保角度来讲,要处理NaNO2,所用物质的还原性应该比KI更强。
点评:该题是基础性试题的考查,主要是考查学生对氧化还原反应的判断、配平以及计算的了解掌握情况。该题的关键是准确标出有关元素的化合价变化情况,然后结合题意和电子得失守恒灵活运用即可,难度不大。
本题难度:一般
3、填空题 印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式如下: Cu + 2 FeCl3 === CuCl2 + 2 FeCl2
(1)请用双线桥法在上式中标出电子转移的情况
(2)此反应中的氧化剂是__________
(3)写出此反应的离子方程式:____________
(4)试比较Fe3+、Cu2+、Fe2+氧化性的强弱:__________ >__________ >_________
参考答案:(1)“略”
(2)FeCl3
(3)Cu + 2 Fe2+ === Cu2+ + 2 Fe2+
(4)Fe3+>Cu2+>Fe2+
本题解析:
本题难度:一般
4、计算题 写出符合下列条件的氧化还原反应方程式
A.一种单质氧化另一种单质
B.一种单质氧化一种化合物
C.一种化合物氧化另一种化合物
D.一种化合物氧化一种单质
参考答案:A.C+O2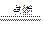 CO2, B.2CO+O2
CO2, B.2CO+O2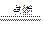 2CO2,C.MnO2+4HCl(浓)
2CO2,C.MnO2+4HCl(浓)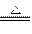 ?MnCl2+Cl2↑+2H2O,D.CuO + H2
?MnCl2+Cl2↑+2H2O,D.CuO + H2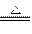 Cu+H2O。
Cu+H2O。
本题解析:本题能力层次为C。甲物质氧化乙物质时,甲物质得到电子,有元素的化合价降低,乙物质失去电子,有元素的化合价升高。
学法指导:氧化还原反应的本质是电子的转移(得失或偏移)。表现为反应前后元素的化合价发生改变,故化合价是分析氧化还原反应的基础。氧化剂具有氧化性,能氧化其他物质,含有化合价降低的元素。
本题难度:简单
5、选择题 下列有关硫化亚铁跟浓硫酸反应的方程式正确的是()
A.2FeS+6H2SO4=Fe2(SO4)3+3SO2↑+2S+6H2O
B.4FeS+18H2SO4=2Fe2(SO4)3+9SO2↑+7S+18H2O
C.6FeS+16H2SO4=3Fe2(SO4)3+6SO2↑+7S+16H2O
D.8FeS+18H2SO4=4Fe2(SO4)3+3SO2↑+11S+18H2O
参考答案:A
本题解析:有的同学只是机械地分析反应前后各元素的原子总数是否守恒,得出四个反应式都正确的错误结论。这是以氧化还原反应为背景考查质量守恒定律。四个反应中氧化剂都是硫酸,还原剂都是硫化亚铁,氧化产物都是单质硫和硫酸铁,还原产物都是二氧化硫。所以反应物FeS中的铁、硫元素与产物Fe2(SO4)3中的铁、单质S中的硫元素守恒,四个选项中,只有A选项中还原剂(FeS)与氧化产物(S)相对应。
本题难度:一般