1、选择题 下列根据实验操作和现象所得出的结论正确的是(?)
?
| 实验操作
| 现象
| 解释或结论
|
A
| 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液
| 出现白色沉淀
| 溶液X中一定含有SO
|
B
| 等体积pH=3的HA和HB
两种酸分别与足量的锌反
应,排水法收集气体
| HA放出的氢气多且反应速率快
| HB酸性比HA强
|
C
| 在镁、铝为电极,氢氧化钠为电解质的原电池装置中
| 镁表面有气泡
| 金属活动性:Al>Mg
|
D
| 向1 mL 1%的NaOH溶液中
加入2 mL 2%的CuSO4溶
液,振荡后加入0.5 mL有
机物Y,加热
| 未出现砖红色
沉淀
| Y中不含有醛基
|
?
参考答案:B
本题解析:A项,SO离子干扰;B项,酸越弱,浓度越大,放出H2的速率越快;C项,Mg的活动性大于铝,不能根据该原电池判断;D项,配制Cu(OH)2悬浊液,应使碱
过量。
本题难度:一般
2、填空题 (14分)某无色溶液X,K+、Ba2+、Al3+、Fe3+、[Al(OH)4]-、CO32-、SO42-中的若干种离子组成,取该溶液进行如下实验:
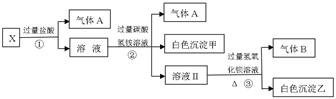
(1)气体A的成分是?(填化学式,下同),气体B的成分是?。
(2)写出步骤①中产生气体的离子方程式?。
(3)分别写出形成白色沉淀甲和气体B的离子方程式
?;?。
(4)通过上述实验,可确定X溶液中一定存在的离子是?,
尚未确定是否存在的离子是?,只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是?。
参考答案:(1)CO2? NH3
(2)CO32- + 2H+ ==CO2↑+ H2O
(3)Al3+ + 3HCO3-= Al(OH)3↓ + 3CO2↑;NH4++OH-=NH3↑+ H2O
(4)K+、 [Al(OH)4]-、CO32-; SO42-;?向沉淀乙加入足量的HCl,如果沉淀完全溶解说明没有SO42-,如果沉淀部分溶解说明有SO42-
本题解析:略
本题难度:简单
3、填空题 (1)衣服上沾有动、植物油污,用水洗不掉,但可用汽油洗去,这是因为大多数有机物难______而易______.有机化工厂附近严禁火种,这是因为绝大多数有机物______.
(2)为了检验和除去下表中的各种物质中的杂质(括号里的物质),请从( I)中选出适当的检验试剂,从( II)中选出适当的除杂试剂,将所选的答案填入相应的空格内.
( I)检验的试剂:A.无水硫酸铜B.酸性高锰酸钾溶液C.盐酸D.氢氧化钠溶液
( II)除杂试剂:a.硫酸?b.酸性高锰酸钾溶液?c.新制的生石灰d.溴水
| 物质 | 检验试剂 | 除杂试剂
甲烷(乙烯)
酒精(水)
参考答案:(1)大多数有机物难溶于水,易溶于有机溶剂,动、植物油属于油脂,不溶于水,溶于有机溶剂,故用水洗不掉,但可用汽油洗去,大多数有机物易燃烧,有机化工厂附近严禁火种,
故答案为:溶于水;溶于有机溶剂;易燃烧;
(2)乙烯能使酸性高锰酸钾溶于褪色,甲烷不可以,可以检验乙烯存在;甲烷不能与溴水反应,乙烯可以与溴水发生加成反应,可以利用溴水除去甲烷中的乙烯;
无水硫酸铜吸水变蓝色,据此检验水的存在,用新制的生石灰吸水蒸馏除去酒精中的水,
故答案为:物质检验试剂除杂试剂甲烷(乙烯)酸性高锰酸钾溶液溴水酒精(水)无水硫酸铜新制的生石灰.
本题解析:
本题难度:简单
4、选择题 下列实验方案合理的是
A.检验混合离子溶液中的SO42-:加入HCl酸化的Ba(NO3)2溶液,观察有无白色沉淀生成
B.除去NO中混有的少量NO2:将混合气体通入水中,再用排空气法收集NO
C.配制浓度为0.1mol/L的NaOH溶液:将0.05molNaOH溶于500mL水配成溶液
D.检验氯化铁溶液中是否混有Cu2+:纸上层析后用氨熏
参考答案:D
本题解析:略
本题难度:一般
5、选择题 为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
?
| 被提纯的物质
| 除杂试剂
| 分离方法
| A
| 乙酸乙酯(乙酸)
| CCl4
| 萃取、分液
| B
| 乙烷(乙烯)
| 高锰酸钾溶液
| 洗气
| C
| 乙醇(乙酸)
| 新制氧化钙
| 蒸馏
| D
| 苯(溴)
| 碘化钾溶液
| 分液
参考答案:C
本题解析:略
本题难度:一般
|
|