1、选择题 欲将苯、硝基苯、己烯鉴别开来,选用的试剂最好是
A.溴水
B.石蕊试液
C.KOH溶液
D.水
参考答案:A
本题解析:考查物质的鉴别。苯和四氯化碳都能萃取溴单质,其中苯在上层,四氯化碳在下层,而己烯中含有碳碳双键,能和溴水发生加成反应,所以选项A正确,其余都是错误的,答案选A。
本题难度:困难
2、填空题 下列各组物质中,属于同位素的是___________,属于同素异形体的是___________,互为同系物的是___________,属于同分异构体的是___________,属于同种物质的是___________。
①O2和O3?②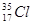 和
和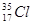 ?③CH3CH2CH2CH3和CH3CH(CH3)2
?③CH3CH2CH2CH3和CH3CH(CH3)2
④CH3CH2CH2CH(C2H5)CH3和CH3(CH2)2CH(CH3)CH2CH3?⑤CH3(CH2)3CH3和CH3CH3
⑥?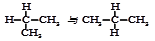
参考答案:②?①?⑤?③?④⑥
本题解析:结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称同系物;分子式相同结构不同的化合物互称同分异构体;质子数相同中子数不同的同一元素的不同原子互称同位素,同位素必须原子;同一元素形成的不同单质称同素异形体,同素异形体必须是单质;所以属于同位素的是②,属于同素异形体的是① ,互为同系物的是⑤ ,属于同分异构体的是③,属于同种物质的是④⑥。
点评:本题考查了同系物、同位素等概念,属于对基础知识的考查,本题比较容易。
本题难度:一般
3、选择题 已知X为第三周期元素的原子,该原子要达到8电子稳定结构,则需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是(?)
A.X元素最高价氧化物对应的水化物一定是强酸
B.X元素的氢化物的化学式一定为H2X
C.X的单质一定是良好的半导体材料
D.X元素的氧化物一定能与烧碱反应
参考答案:D
本题解析:第三周期元素的次外层有8个电子,最内层有2个电子,二者之差为6。因为该原子达到8电子稳定结构需要的电子数小于6,则需要的电子数为2或4。若为2,则X为S;若为4,则X为Si,硅酸为弱酸,A错;硅的氢化物为SiH4,B错;S单质不能作半导体材料,C错;SO2、SO3和SiO2都能与烧碱反应,D正确。
本题难度:一般
4、选择题 除去NaCl中混有的 MgCl2、Na2SO4时选用
A.NaOH、Ba(NO3) 2、Na2CO3、HCl
B.Ca(OH) 2、Mg(NO3) 2、Na2CO3、HCl
C.NaOH、BaCl2、Na2CO3、HCl
D.Na2CO3、BaCl2、HCl
参考答案:C
本题解析:试题分析:因为反应要在溶液中进行,所以要先配制成溶液,然后除去硫酸根离子,再除钙离子和镁离子,最后加入盐酸除去过量的碳酸根和氢氧根.
故答案为:(1)将粗盐溶于足量水中制成溶液.
(2)向上述溶液中加入足量的BaCl2溶液,除去SO42-,Na2SO4+BaCl2=BaSO4↓+2NaCl,过滤,除去滤渣.
(3)向上述虑液中加入足量的Na2CO3溶液,除去Ba2+, Na2CO3+BaCl2=BaCO3↓+2NaCl,过滤,除去滤渣.
(4)向(3)虑液中加入足量的NaOH溶液,除去Mg2+,2NaOH+MgCl2=Mg(OH)2↓+2NaCl,过滤,除去滤渣.
(5)向(4)虑液中滴加稀盐酸,调节PH=7,除去CO32-和OH-,Na2CO3+2HCl=H2O+CO2↑+2NaCl,NaOH+HCl=NaCl+H2O.
(6)将NaCl溶液蒸发,洗涤干燥,即得较纯净的食盐。
故选C。
考点:物质除杂或净化的探究 盐的化学性质
点评:除杂一般有两种方法,将杂质彻底除去或将杂质转化为主物质,所选物质不能与主物质发生反应,也不要在除去杂质的同时又混入了其它物质。要注意除杂质的顺序。
本题难度:简单
5、选择题 A、B、C、D、E、F六种元素在周期表中的位置如图所示,下列说法正确的是(?)
族
周期
| IA
| ?
| 0
|
1
| A
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| ?
|
2
| ?
| ?
| ?
| ?
| ?
| ?
| D
| ?
|
3
| B
| ?
| ?
| ?
| E
| C
| F
| ?
|
A.热稳定性:A2C>AD?
B.EF3分子中所有原子均达到8电子稳定结构,且属于非极性分子
C.六种元素中的某些元素可以形成既含共价键又含离子键的化合物
D.晶体熔点:BF<BD
参考答案:CD
本题解析:略
本题难度:简单