1、选择题 若某ⅡB族原子序数为x,那么原子序数为x+1的元素位于(?)
A.ⅢB族
B.ⅢA族
C.ⅠB族
D.ⅠA族
2、填空题 X、Y、Z是三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物。已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多1个电子层。
(1)X离子的结构示意图为________。
(2)Z2Y对应水化物的碱性比LiOH________。
(3)Z2X属于________(填“共价”或“离子”)化合物。
(4)Z2Y2中含有________键和________键,Z2Y2溶于水时发生反应的化学方程式是__________________________________________________________________。
3、选择题 下列说法正确的是(?)
A.IA族元素的金属性一定比IIA族元素的金属性强
B.ⅥA族中氢化物最稳定的元素,其最高价含氧酸的酸性也最强
C.某一元素可能既显金属性,又显非金属性
D.短周期中,同周期元素所形成的简单离子的半径,从左到右逐渐减小
4、选择题 下列物质属于混合物的是
A.硫酸
B.盐酸
C.硝酸
D.冰水混合
5、填空题 (16分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语
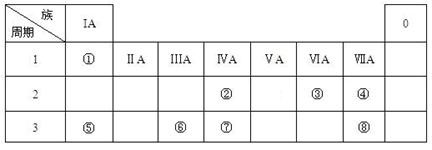
回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为_______________________,②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是______________________。
(2)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl 3 c.Na2SO3 d.KMnO4
若已知1 克该液态化合物分解成③的单质和一种常见液体时,可放出2.9kJ能量,写出该反应的热化学方程式:?
(3)工业上常采用电解A和冰晶石(Na3AlF6)混合物的方法冶炼制备⑥的单质,请从A晶体的类型和微粒间的相互作用力角度解释加冰晶石(Na3AlF6)的原因?。?并写出电解时的电极反应式:?。
(4)甲、乙、丙是上述部分元素组成的双原子分子或负二价双原子阴离子,且甲、乙、丙的电子总数相等。甲是一种极强的氧化性单质。丙与⑤的阳离子可形成一种淡黄色固体B,该固体跟水反应可得到③的单质。则B电子式?,乙的结构式?,甲的组成元素的原子结构示意图?,能证明甲的组成元素非金属性很强的事实?。(任举一例即可)