1、选择题 从下列事实所得出的解释或结论正确的是
选项
| 实验事实
| 解释或结论
|
A
| 2N2O5(g) 4NO2(g)+O2(g)?ΔH>0 4NO2(g)+O2(g)?ΔH>0
在室温下能自发进行
| 这是一个熵增的反应
|
B
| 压缩针筒内的NO2和N2O4混合气体,
颜色先变深后变浅
| 增大压强,平衡向生成N2O4的方向移动,新平衡比旧平衡压强小
|
C
| 锌与稀硫酸反应过程中,开始反应后速率逐渐增大
| 该反应是放热反应
|
D
| 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动
| 反应物的浓度一定降低
|
?
参考答案:AC
本题解析:A、根据反应方向的判据ΔH―TΔS判断,反应自发进行ΔH―TΔS<0,该反应ΔH>0,则只有ΔS>0时能自发进行,正确;B、根据平衡移动原理知,平衡移动只能减弱条件的改变,不能抵消,增大压强,平衡向生成N2O4的方向移动,新平衡比旧平衡压强大,错误;C、锌与稀硫酸反应过程中,开始反应后速率逐渐增大,只能是温度升高,反应速率加快,该反应为放热反应,正确;D、若增大反应物的浓度使平衡正向移动,反应物的转化率不一定增大,错误。
本题难度:一般
2、选择题 恒温恒容条件下,下列叙述中不是可逆反应2A(g)+3B(s)?2C(g)达到平衡的标志的是( )
①C的生成速率与C的分解速率相等;
②单位时间生成amolA,同时消耗1.5amolB;
③各组分的浓度不再变化;
④混合气体的密度不再变化;
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦混合气体的平均摩尔质量不再变化;
⑧A、B、C的分子数目比为2:3:2.
A.⑤⑥⑧
B.②⑤⑧
C.①③④
D.②④⑦
参考答案:①C的生成速率与C的分解速率相等,正逆反应速率相等,达到了化学平衡,故①不可选;
②单位时间生成amol A,代表逆反应速率,同时消耗1.5amol B,代表正反应速率,且物质的量的变化之比等于化学计量数之比,因此逆反应和正反应速率相等,达到了化学平衡,故②不可选;
③A、B、C的浓度不再变化,达到了平衡状态,故③不可选;
④由于B为固体,因此反应前后气体的质量变化,恒容气体的总体积不变,所以密度变化,因此混合气体的密度不再变化说明达到平衡状态,故④不可选;
⑤应前后气体的化学计量数相等,因此在恒温恒容条件下压强是一定值,混合气体的总压强不再变化不能说明达到平衡状态,故⑤可选;
⑥反应前后气体的化学计量数相等,对于气体物质而言此反应属于等物质的量的反应,因此混合气体的物质的量不再变化不能说明达到平衡状态,故⑥可选;
⑦反应前后气体的化学计量数相等,物质的量不变,由于B为固体,因此反应前后气体的质量变化,因此混合气体的平均摩尔质量为以变化的值,当混合气体的平均摩尔质量不再变化说明达到平衡状态,故⑦不可选;
⑧A、B、C的分子数目比为2:3:2,既不能说明各组分的浓度不再变化,又不能逆反应和正反应速率相等,因此不能说明达到化学平衡状态,故⑧可选;
故选:A.
本题解析:
本题难度:一般
3、选择题 下列事实,不能用勒复夏特列原理解释的是?(?)
A.氨水中加酸,NH4+ 的浓度增大
B.合成氨工业中不断从反应混合物中液化分离出氨气
C.实验室中常用排饱和食盐水的方法收集Cl2
D.合成氨控制在500℃左右的温度
参考答案:D
本题解析:略
本题难度:简单
4、填空题 (17分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上采用如下反应合成甲醇:
CO(g)+2H2(g) CH3OH(g),现模拟并分析该反应:
CH3OH(g),现模拟并分析该反应:
(1)能够说明该反应已达到平衡的是_________:
a.恒温、恒容时,容器内的压强不再变化
b.恒温、恒容时,容器内混合气体的密度不再变化
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗2molH2的同时生成1 mol CH3OH
(2)右图是该反应在不同温度下CO转化率随时间的变化曲线:

①该反应的△H____0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数:K1____K2(填“>”、“<”或“=”)。
(3)2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如图1所示。
①甲醇完全燃烧的化学方程式_______________________。
②请写出从C口通入O2发生的电极反应式___________________。
(4)用上述电池做电源,用图2装置电解饱和食盐水(C1、C2均为石墨电极)。
①该反应的离子方程式________________________。
②电解开始后在电极__________________的周围(填“C1”或“C2”)先出现红色。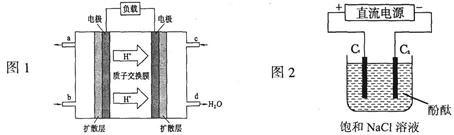
参考答案:(1)ac(4分(4分,选一个对得2分,一对一错不得分):
(2)①<(2分)?②>(2分)
(3)①2CH3OH+3O2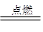 2CO2+4H2O(2分);②O2+4e-+4H+=2H2O(2分)
2CO2+4H2O(2分);②O2+4e-+4H+=2H2O(2分)
(4)2Cl-+2H2O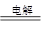 Cl2↑+H2↑+2OH-(3分)? C2?(2分)
Cl2↑+H2↑+2OH-(3分)? C2?(2分)
本题解析:(1)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以c正确。根据方程式可知,反应是体积减小的,因此压强也是减小的,所以a也能说明达到平衡状态。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,b不正确。D中反应速率的方向是相同的,不正确。答案选ac。
(2)①根据图像可知,温度为t2的曲线首先达到平衡状态,说明反应速率快,因此t2大于t1。温度高,CO的转化率低,说明升高温度,平衡向逆反应方向移动,因此正反应是放热反应,即△H<0。
②升高温度,平衡向逆反应方向移动,因此平衡常数减小,即K1>K2。
(3)①甲醇完全燃烧的生成物是水和CO2。所以方程式为2CH3OH+3O2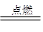 2CO2+4H2O。
2CO2+4H2O。
②氧气在反应中得到电子,因此在正极通入,又因为氢离子向正极移动,所以正极电极反应式为O2+4e-+4H+=2H2O。
(4)惰性电极电解饱和食盐水时,阳极是氯离子放电,产生氯气。阴极是氢离子放电,产生氢气,因此阴极周围水的电离平衡被破坏,溶液显碱性,显红色。由于C2和电源的负极相连,所以
C2是阴极,该电极周围溶液显红色。该反应的方程式为2Cl-+2H2O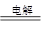 Cl2↑+H2↑+2OH-。
Cl2↑+H2↑+2OH-。
本题难度:一般
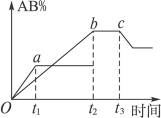
5、选择题 有反应A2+B2 2AB;在温度和压强可变条件下,产物AB的生成情况如图所示:a为500 ℃,b为300 ℃,从t3开始压缩容器,则下列叙述正确的是
2AB;在温度和压强可变条件下,产物AB的生成情况如图所示:a为500 ℃,b为300 ℃,从t3开始压缩容器,则下列叙述正确的是
A.AB为气体,A2、B2中必有一种为非气体;正反应吸热
B.AB为气体,A2、B2中必有一种为非气体;正反应放热
C.AB为固体,A2、B2中必有一种为非气体;正反应放热
D.A2、B2、AB均为气体;正反应吸热
参考答案:B
本题解析:据图象知,500 ℃比300 ℃时生成物AB的百分含量低,说明正反应为放热反应,A项、D项一定不正确。同一温度下,从t3开始压缩容器即增大压强,生成物AB百分含量减小,则说明平衡逆向移动,正反应是体积增大的反应,C项属于体积减小的反应,不符合题意。答案为B项。
本题难度:简单