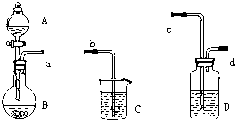
1、简答题 实验室中可用如下所示装置验证乙酸、碳酸和石炭酸三者的酸性相对强弱.
请你思考后回答下列问题:
(1)写出下列仪器中所盛装的试剂:
A______,B______,C______.
(2)你认为装置D中装的试剂可能是______溶液,它的作用是:______.
(3)请你选用上述仪器组装成一套装置,可以直接验证上述三种物质的酸性强弱,仪器接口顺序为:a→______.
(4)实验中在烧杯中C中可以观察到的现象应该是______,写出反应的化学方程式:______.
2、实验题 (12分)某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙两套装置(图中的夹持仪器均未画出,“△”表示酒精灯热源),每套装置又可划分为①、②、③三部分。仪器中盛放的试剂为:a―无水乙醇(沸点:78℃);b―铜丝;c―无水硫酸铜;d―新制氢氧化铜悬浊液。
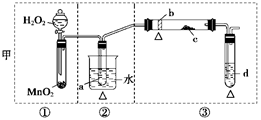
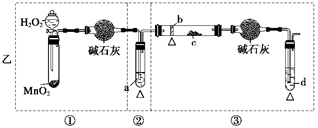
(1)简述两套方案各自的优点:
甲:__________________________________________________________________,
乙:___________________________________________________________________。
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为_________________________________________________________(例如甲①,乙②)。
(3)若要保证此实验有较高的效率,还需补充的仪器有________,理由_______________。
(4)实验中能验证乙醇氧化产物的实验现象是________________________________。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式:__________________________________。
3、选择题 甲酸的下列性质中,可以证明它是弱电解质的是( )
A.甲酸溶液使紫色石蕊试液变红
B.甲酸能与水以任何比例互溶
C.10mL?1?mol/L甲酸恰好与10mL?1?mol/L?NaOH的溶液完全反应
D.1mol/L甲酸溶液的pH约为2
4、填空题 (12分)不同的金属在化学反应中表现出来的活泼程度不同,俄国化学家贝开托夫在大量实验和系统研究之后,于1865年发表了金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 。
(1)金属活动性顺序是学习“金属及其化合物”的重要工具,许多“金属及其化合物”的知识规律可以通过金属活动性顺序来掌握。例如,工业上冶炼金属,根据金属 活动性顺序可以采用不同的冶炼方法。其中可以用“热分解法”冶炼的金属是__________、?。
活动性顺序可以采用不同的冶炼方法。其中可以用“热分解法”冶炼的金属是__________、?。
工业上又常用下列反应进行金属钾的冶炼: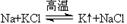 ,似乎“违背”了金属活动性顺序,试解释钠能将更活泼的钾置换出来的原因__________________________ 。
,似乎“违背”了金属活动性顺序,试解释钠能将更活泼的钾置换出来的原因__________________________ 。
(2)在实践中发现还有许多化学事实 “违背”金属活动性顺序,但这些“反常”现象都可以通过化学原理得到合理解释。某学生在做探究实验时,把锌粒投入1mol・L-1氯化铁溶液中,观察到如下实验现象:锌粒表面有一定 量气泡产生,溶液颜色逐渐变浅,一段时间后溶液
量气泡产生,溶液颜色逐渐变浅,一段时间后溶液 逐渐浑浊,试用相关反应方程式进行解释_________________________________、
逐渐浑浊,试用相关反应方程式进行解释_________________________________、
__________________________________________________________________________。
(3)研究金属活动性顺序还可以指导对金属阳离子氧化性强弱的认识,工业上用氯化铁溶液腐蚀铜制电路板。
①请根据金属活动性顺序结合该反应原理,比较Cu2+、Fe3+、Fe2+的氧化性强弱?。
②请运用原电 池原理设计实验验证Cu2+、Fe3+氧化性强弱的结论。
池原理设计实验验证Cu2+、Fe3+氧化性强弱的结论。
方案___________________________ ___________________________________________。
___________________________________________。
5、填空题 某学生设计下列实验来制取、检验HCl气体溶水性及证明酸性:盐酸>碳酸>苯酚
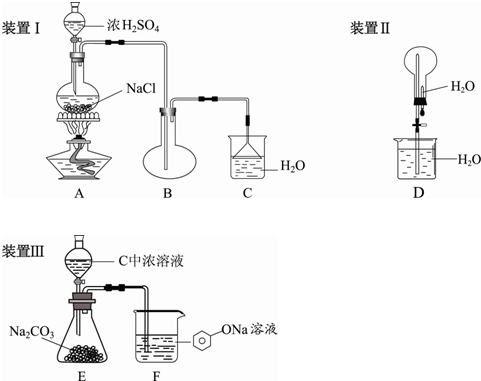
(1)装置III的实验目的是______.
(2)装置I倒置漏斗的作用是______.
(3)如何检验装置II的气密性______.“喷泉”实验的操作方法是______.
(4)装置III要达到实验目的有设计上的不足,请设计出改进方案______.
(5)写出F中反应的离子方程式______,F装置的溶液中电荷守恒的离子浓度关系式______.