1��ʵ���� ��8�֣�ij��ѧ��ȤС���ڼ� �������������������ܱ������и�����һ������̼�ۣ��ڸ���������ʹ���ַ�Ӧ������Ӧ���������������е�̼�۶�����ȫ��ʧ����С���Ա�Է�Ӧ���������������������̽����
�������������������ܱ������и�����һ������̼�ۣ��ڸ���������ʹ���ַ�Ӧ������Ӧ���������������е�̼�۶�����ȫ��ʧ����С���Ա�Է�Ӧ���������������������̽����
��С��ͬѧ�Լ�������������������������ֲ��룺
��ֻ��CO?��ֻ��CO2?��ֻ��O2?��CO��O2�Ļ������
����Ϊ�������������Բ���������?������ţ�
��С��ͬѧ��Ϊ�������е����廹������CO��CO2�Ļ������,Ϊ����֤�Լ��IJ��룬��������ͼ��ʾװ�ý���̽����
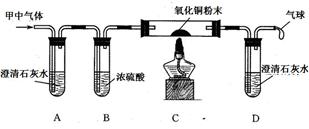
����ش��������⣺
��С���IJ����������װ��A�з�Ӧ�Ļ�ѧ����ʽ��?��װ��C�������е�ʵ��������??����Ӧ�Ļ�ѧ����ʽ��?��
��С��ͬѧ����������������������˳��������������һ�ֺ������룬���IJ�����?�����������������ʵ�鷽����֤����룺
������1���ȼ���װ��ͭ˿���IJ�����һ��ʱ�����ͨ�����е����壬�۲�����
������2�������е�����ͨ�����ʯ��ˮ���۲�����
ָ����ʦ�ڷ�����ʵ�鷽����ָ�������д��ڵĴ�����㡣
�ٲ���1Ӧ��ͨ����������һ��ʱ��ɼ��ȡ�����Ϊ�����ĵ�ԭ����?��
��û�б�Ҫ�� �в���2��ʵ�飬��������?��
�в���2��ʵ�飬��������?��
������Ӧǰ�ס�����������̼���������������ȷֱ��ʾΪ(mC/mO2)��
��(mC/mO2)�ң���С����С���IJ��������ʱ����(mC/mO2)��__________
(mC/mO2)�ң����������������=������
2��ʵ���� ��15�֣�����������һ�ֳ���ʳƷ���Ӽ���Ϊ����ijʳƷ���������κ�����ͨ��1kg��Ʒ�к�SO2�������ƣ���ij�о�С���������������ʵ�����̣�

��1������A����Ҫ�ɷ���?��Ϊ��ֹ���ʱ�������У�����������ƿ�м���?
?��ͨ��N2��Ŀ����?��
��2��д�������ڢٲ���Ӧ�����ӷ���ʽ��?��
��3�������ڢڲ��ζ�ǰ���ζ�������NaOH����Һ��ϴ�������������?
?��
��4�������������ϡ���ᴦ����Ʒ�����ҷ���ʵ��ⶨ�Ľ��?���ƫ�ߡ�����ƫ�͡�����Ӱ�족��
��5����ȡ��Ʒwg�����ҷ����������0.01000mol��L��1I2��ҺVmL����1kg��Ʒ�к�SO2��������?g���ú�w��V�Ĵ���ʽ��ʾ����
3��ѡ���� �������ʵļ��飬�����һ����ȷ���ǣ�������
A��ij��Һ�м���BaCl2��Һ��������ɫ����������HNO3�������ܽ⣬�����Һ��һ������SO42-
B��ij��Һ�м��������ܲ���ʹ����ʯ��ˮ����ǵ����壬�����Һ��������SO32-��CO32-�е�һ��
C��ȡ����Na2SO3��Ʒ���Թ��м�ˮ�ܽ���������������������ټ���BaCl2��Һ�а�ɫ����������˵��Na2SO3��Ʒ�Ѳ��ֱ�����
D����ʹʪ��ĵ⻯�ص�����ֽ������һ����Cl2
4��ѡ���� ���л�ѧʵ����ʵ������Ͷ���ȷ����
A��������ͭм��ϡ�������ã���Ӧֹͣ���ټ���1mol/Lϡ���ᣬͭм�����ܽ�����Ϊͭ��ֱ����1mol/Lϡ���ᷴӦ
B����������Ũ�����н��ݺ���������ˮ��ϴ��Ȼ�����CuSO4��Һ�в���Ӧ��˵�����������γ���һ�������ȶ�������Ĥ
C����п��ϡ���ᷴӦ�������ȴ�п�죬����Ϊ��п�ȴ�п��ԭ��ǿ
D����ҵ�Ʋ�������Ҫ��Ӧ֮һ��������Na2CO3+SiO2=Na2SiO3+CO2��