1、选择题 下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是( )
A.10℃3mol/L的盐酸溶液
B.20℃2mol/L的盐酸溶液
C.10℃4mol/L的盐酸溶液
D.20℃4mol/L的盐酸溶液
参考答案:根影响化学反应速率的因素:温度越高反应速率越快,所以A、C的最慢;浓度越大,反应速率越快,所以D最快.
故选D.
本题解析:
本题难度:简单
2、填空题 (5分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)(2分)硫酸铜溶液可以加快氢气生成速率的原因 。
(2)(1分)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是 。
(3)(2分)要加快上述实验中气体产生的速率,还可采取的措施有(答两种): ; 。
参考答案:(1)CuSO4与Zn反应生成的Cu附着在Zn表面形成铜锌原电池加快了化学反应速率;
(2)Ag2SO4;
(3)适当增加硫酸的浓度;增加锌粒的表面积;升高温度等(答两种即可)。
本题解析:(1)硫酸铜溶液可以加快氢气生成速率的原因是CuSO4与Zn反应生成的Cu附着在Zn表面形成铜锌原电池加快了化学反应速率。
(2)Ag2SO4与Zn反应生成的Ag附着在Zn表面形成银锌原电池加快了化学反应速率,所以与上述实验中CuSO4溶液起相似作用的是Ag2SO4;
(3)根据影响化学反应速率的因素可知,要加快上述实验中气体产生的速率,还可采取的措施有:适当增加硫酸的浓度;增加锌粒的表面积;升高温度等。
考点:理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,认识并能用相关理论解释其一般规律。
点评:本题考查了影响化学反应速率的因素,特别是原电池对化学反应速率的影响。
本题难度:一般
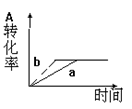
3、选择题 已知某可逆反应在密闭容器中进行:A(g)+2B(g)  3C(g)+D(s) △H<0,下图中曲线a 代表一定条件下该反应的过程,若使a曲线变为b曲线,可采用的措施是(?)
3C(g)+D(s) △H<0,下图中曲线a 代表一定条件下该反应的过程,若使a曲线变为b曲线,可采用的措施是(?)
A.增大A的浓度
B.增大容器的体积
C.加入催化剂
D.升高温度
参考答案:C
本题解析:由图可以看出,反应速率加快,缩短了达到化学平衡所需要的时间,但平衡时A的转化率没变。说明平衡没有发生移动。只有加入催化剂这种措施。
本题难度:一般
4、实验题 某探究小组用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速度的因素。
实验药品:2.0 mol/L盐酸、4.0 mol/L盐酸、2.0 mol/L硫酸、4.0 mol/L硫酸、相同大小的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0 mL,金属用量均为9.0 g。
Ⅰ.甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
反应进程
(分钟)
| 1
| 2
| 5
| 15
| 20
|
4.0 mol/L
盐酸
| 少量气泡
| 较多气泡
| 大量气泡
| 反应剧烈
| 铝片耗尽
|
2.0 mol/L
硫酸
| 无明显现象
| 极少量
气泡
| 少量气泡
|
4.0 mol/L
硫酸
| 无明显现象
| 少量气泡
| 有比较连续的气泡
|
?
请回答下列问题:
(1)写出铝与盐酸反应的离子方程式:?。
(2)反应在1~15min内,铝与盐酸的反应速率逐渐增大,其原因是?。
(3)根据以上探究“铝与稀盐酸和稀硫酸的反应速率存在差异的原因”,你能对原因作出哪些假设或猜想:?(写出一种即可)。
Ⅱ.乙同学设计了如下影响反应速率因素的实验。请你根据实验目的帮助该同学完成以下实验设计表:
实验目的
| 实验
编号
| 温度
/℃
| 金属铝的
形态
| 盐酸浓度
/mol・L-1
|
1.实验①和②探究盐酸浓度对该反应速率的影响;
2.实验①和③探究温度对该反应速率的影响;
3.实验①和④探究金属规格(铝片、 铝粉)对该反应速率的影响
| ①
| 25
| 铝片
| 4.0
|
②
| ?
| ?
| ?
|
③
| ?
| ?
| ?
|
④
| ?
| ?
| ?
|
?
参考答案:Ⅰ.(1)2Al+6H+=2Al3++3H2↑ (2)反应放出热量,温度升高,使化学反应速率加快 (3)Cl-能够促进金属铝与H+的反应(或SO42-对H+与金属铝的反应起阻碍作用) Ⅱ.如下表所示:
实验编号
温度/℃
金属铝的形态
盐酸浓度/mol・L-1
②
25
铝片
2.0
③
50
铝片
4.0
④
25
铝粉
4.0
?
注:③中温度填其他合理答案也可
本题解析:Ⅰ.(2)1~15 min内铝与盐酸的反应速率逐渐增大的原因主要与反应温度有关,因为该反应是放热反应。(3)比较第1组和第2组(相同H+浓度的盐酸和硫酸),二者的区别在于阴离子不同,从而导致反应速率差别较大,故可得出有关假设:Cl-能够促进金属铝与H+反应或SO42-对H+与金属铝的反应起阻碍作用。Ⅱ.要完成实验设计,必须明确对比实验的目的。因为实验①和②是探究盐酸浓度对该反应速率的影响,故只改变②中盐酸的浓度;实验①和③是探究温度对该反应速率的影响,故只改变③中的反应温度;实验①和④是探究金属规格(铝片、铝粉)对该反应速率的影响,故只改变④中金属铝的形态。
本题难度:一般
5、选择题 反应C (s) + H2O (g) 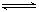 CO(g) + H2 (g)在一可变容积的密闭容器中进行,下列条件的改变能加快其反应速率的是(?)
CO(g) + H2 (g)在一可变容积的密闭容器中进行,下列条件的改变能加快其反应速率的是(?)
A.保持体积不变,充入N2使体系压强增大
B.增加C的量
C.保持压强不变,充入N2使容器体积变大
D.将容器的体积缩小一半
参考答案:D
本题解析:考查外界条件对反应速率的影响。保持体积不变,充入N2使体系压强增大,但物质的浓度是不变的,反应速率不变;碳是固体,改变固体的质量,反应速率不变;保持压强不变,充入N2使容器体积变大,则物质的浓度必然减小,因此反应速率降低。将容器的体积缩小一半,压强增大,物质的浓度也是增大的,反应速率增大,因此正确的答案选D。
本题难度:一般