1、简答题 已知:①HSO3-的还原性比I-强,②IO3-+5I-+6H+=3I2+3H2O.工业上利用NaIO3和NaHSO3反应来制取单质I2.NaIO3来源于自然界的矿物,NaHSO3来源于硫酸工厂尾气处理的产物(用NaOH溶液吸收SO2).
(1)配平下列第②个反应,将系数填在横线上.
①NaIO3不足时,发生反应:2NaIO3+6NaHSO3=2NaI+3Na2SO4+3H2SO4
②NaIO3足量时,发生反应:______NaIO3+______NaHSO3=______I2+______Na2SO4+______H2SO4+______H2O
(2)现模拟工业制取I2.在含5molNaHSO3的溶液中逐滴加入NaIO3溶液.请画出加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线.
(3)若工业上要生产2.54吨I2,至少需要处理标准状况下SO2的体积分数为0.224%的硫酸厂的尾气多少立方米?
参考答案:(1)化学反应中碘元素化合价从+5价降为0价,生成1mol碘单质共降低10价,硫元素的化合价从+4价升高到+6价,2molNaHSO3生成1molNa2SO4共升高了4价,根据电子守恒和原子守恒,则碘酸钠的前面系数是4,亚硫酸氢钠的系数是10,即4NaIO3+10NaHSO3=2I2+7Na2SO4+3H2SO4+2H2O,故答案为:4;10;2;7;3;2;
(2)根据化学方程式4NaIO3+10NaHSO3=2I2+7Na2SO4+3H2SO4+2H2O可以知道加入NaIO3的物质的量和析出I2单质的物质的量的关系是2:1,5molNaHSO3消耗2mol碘酸钠时恰好生成碘单质1mol,即
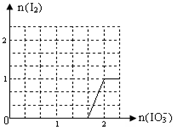
,故答案为:

;
(3)NaOH溶液吸收SO2的反应表示为:SO2+2NaOH=NaHSO3,结合反应4NaIO3+10NaHSO3=2I2+7Na2SO4+3H2SO4+2H2O,可以得到对应关系式:SO2~NaHSO3~0.2I2,假设需要处理标准状况下SO2的体积分数为0.224%的硫酸厂的尾气体积为V,则
SO2~NaHSO3~0.2I2
1?0.2
V?2.54×106254
解得V=5×105(m3)
答:至少需要处理标准状况下SO2的体积分数为0.224%的硫酸厂的尾气5×105m3.
本题解析:
本题难度:一般
2、填空题 实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下:

⑴制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式?。
⑵如图所示,过滤操作中的一处错误是?。判断流程中沉淀是否洗净所用的试剂是?。高温焙烧时,用于盛放固体的仪器名称是?。

⑶在25℃下,向浓度均为0.01 mol?L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成_______沉淀(填化学式),生成该沉淀的离子方程式_______?______________
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10 -34。)
⑷无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

装置B中盛放饱和NaCl溶液,该装置的主要作用是?; F中试剂的作用是?;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为?。
⑸将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为?g。
参考答案:(1)? 2 Al(OH)3+Mg (OH)2 MgAl2O4 + 4H2O?
MgAl2O4 + 4H2O?
(2)漏斗下端尖嘴未紧贴烧杯内壁? AgNO3溶液(或硝酸酸化的AgNO3溶液);坩埚
(3)Al(OH)3?Al3++ 3NH3・H2O=Al(OH)3↓+ 3NH4+
(4)除去HCl;吸收水蒸气;碱石灰(或NaOH与CaO混合物)
(5)8.00
本题解析:
?
?试题分析:(1)向MgCl2、AlCl3的混合溶液中加入过量的氨水,发生反应:MgCl2+ 2NH3・H2O=Mg(OH)2↓+ 2NH4Cl;AlCl3+ 3NH3・H2O=Al(OH)3↓+ 3NH4Cl;然后把Al(OH)3、Mg (OH)2沉淀过滤出来,并洗涤干净、干燥,最后高温灼烧发生反应2Al(OH)3+Mg (OH)2 MgAl2O4 + 4H2O。即得到要制备MgAl2O4。⑵在如图所示的过滤操作中的错误是漏斗下端尖嘴未紧贴烧杯内壁。由于沉淀是从金属氯化物中过滤出来的,所以要判断流程中沉淀是否洗净的方法就是用硝酸酸化的AgNO3溶液来检验是否含有Cl-即可。高温焙烧时,要用坩埚来盛放固体物质。⑶Mg2+形成沉淀需要的
MgAl2O4 + 4H2O。即得到要制备MgAl2O4。⑵在如图所示的过滤操作中的错误是漏斗下端尖嘴未紧贴烧杯内壁。由于沉淀是从金属氯化物中过滤出来的,所以要判断流程中沉淀是否洗净的方法就是用硝酸酸化的AgNO3溶液来检验是否含有Cl-即可。高温焙烧时,要用坩埚来盛放固体物质。⑶Mg2+形成沉淀需要的 ;而Al3+形成沉淀需要的
;而Al3+形成沉淀需要的 <4.242×10-5。需要的OH-的浓度越小,越容易形成沉淀。因此首先形成的是Al(OH)3沉淀。(4)装置B中盛放饱和NaCl溶液,该装置的主要作用是除去氯气中杂质气体HCl,同时减小氯气的溶解。由于无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,所以在F中试剂的作用是吸收水蒸气,防止无水AlCl3水解。用干燥管装填碱石灰也可起到F和G的作用。⑸Mg、Cu与硝酸发生反应变为Mg2+、Al3+时失去的电子的物质的量与HNO3得到电子的物质的量相等。而当向反应后的溶液中加入NaOH溶液金属离子恰好完全沉淀时增加的质量就是OH-的质量,其物质的量就等于Mg2+、Al3+时失去的电子的物质的量。根据等量关系可得。n(NO)= 1.792L÷22.4L/mol=0.08mol.所以n(e-)="0.08mol×3=0.24mol." 故形成沉淀的质量为3.92g+0.24mol×17g/mol=8.00g。考点:
<4.242×10-5。需要的OH-的浓度越小,越容易形成沉淀。因此首先形成的是Al(OH)3沉淀。(4)装置B中盛放饱和NaCl溶液,该装置的主要作用是除去氯气中杂质气体HCl,同时减小氯气的溶解。由于无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,所以在F中试剂的作用是吸收水蒸气,防止无水AlCl3水解。用干燥管装填碱石灰也可起到F和G的作用。⑸Mg、Cu与硝酸发生反应变为Mg2+、Al3+时失去的电子的物质的量与HNO3得到电子的物质的量相等。而当向反应后的溶液中加入NaOH溶液金属离子恰好完全沉淀时增加的质量就是OH-的质量,其物质的量就等于Mg2+、Al3+时失去的电子的物质的量。根据等量关系可得。n(NO)= 1.792L÷22.4L/mol=0.08mol.所以n(e-)="0.08mol×3=0.24mol." 故形成沉淀的质量为3.92g+0.24mol×17g/mol=8.00g。考点:
本题难度:困难
3、填空题 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。 请回答下列问题:
(1)B的原子结构示意图?。
(2)C、D、E三种原子对应的离子半径由大到小的顺序是??(填具体离子);由A、B、C三种元素按4∶2∶3组成的化合物所含的化学键类型为?。
(3)用某种废弃的金属易拉罐与A、C、D组成的化合物溶液反应,该反应的离子方程式为:?。
(4)在100 mL 18 mol/L的浓的A、C、E组成的酸溶液中加入过量的铜片,加热使之充分反应, 产生的气体在标准状况下的体积可能是?(填序号);
a.7.32 L? b.6.72 L? c.20.16 L? d.30.24 L
若使上述反应中剩余的铜片继续溶解,可向其中加入硝酸钠,反应的离子方程式为:?。
(5)A、C两元素的单质与熔融K2CO3组成的燃料电池,其负极反应式为?,用该电池电解1 L 1 mol/L NaCl溶液当消耗标准状况下1.12 L H2时,NaCl溶液的pH=??(假设电解过程中溶液的体积不变)。
参考答案:(1)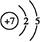 (2)S2->O2->Na+共价键和离子键
(2)S2->O2->Na+共价键和离子键
(3)2Al+2OH-+2H2O=2Al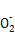 +3H2↑
+3H2↑
(4)ab 3Cu+8H++2N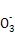 =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O
(5)H2+C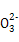 -2e-=CO2↑+H2O ?13
-2e-=CO2↑+H2O ?13
本题解析:由于A和C可形成两种常见的液态化合物,且C的原子序数大,故A为H,C为O,结合C、E为同主族的短周期元素,则E为S;又据A、D最外层电子数相同,故D为Na;再据B、C的最外层电子数之和等于D的原子核外电子数,则B为N。故(1)N的原子结构示意图为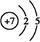 。(2)电子层数越多,离子的半径越大,而电子层结构相同的离子,“核大径小”,故离子半径大小顺序为S2->O2->Na+,由A、B、C三种元素按4∶2∶3组成的化合物是NH4NO3,NH4NO3中含有离子键和共价键。(3)Al和NaOH溶液反应生成NaAlO2和H2,离子方程式为2Al+2OH-+2H2O=2Al
。(2)电子层数越多,离子的半径越大,而电子层结构相同的离子,“核大径小”,故离子半径大小顺序为S2->O2->Na+,由A、B、C三种元素按4∶2∶3组成的化合物是NH4NO3,NH4NO3中含有离子键和共价键。(3)Al和NaOH溶液反应生成NaAlO2和H2,离子方程式为2Al+2OH-+2H2O=2Al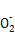 +3H2↑。(4)A、C、E组成的酸为H2SO4,浓H2SO4和Cu反应但稀H2SO4和Cu不反应,故生成SO2的物质的量小于硫酸的一半,根据硫原子守恒知,气体的体积小于20.16 L,故选a、b。若加入NaNO3,提供的N
+3H2↑。(4)A、C、E组成的酸为H2SO4,浓H2SO4和Cu反应但稀H2SO4和Cu不反应,故生成SO2的物质的量小于硫酸的一半,根据硫原子守恒知,气体的体积小于20.16 L,故选a、b。若加入NaNO3,提供的N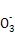 与H+又与Cu反应:3Cu+8H++2N
与H+又与Cu反应:3Cu+8H++2N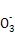 =3Cu2++2NO↑+4H2O。(5)组成的电池是氢氧燃料电池,负极上H2失去电子和C
=3Cu2++2NO↑+4H2O。(5)组成的电池是氢氧燃料电池,负极上H2失去电子和C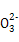 反应生成CO2和水,电极反应式为H2+C
反应生成CO2和水,电极反应式为H2+C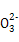 -2e-=CO2↑+H2O。当消耗标准状况下1.12 L H2即n(H2)="0.05" mol,则电解NaCl溶液时消耗H2O电离出的H+的物质的量为0.1 mol,则产生的n(OH-)="0.1" mol,即 c(OH-)=
-2e-=CO2↑+H2O。当消耗标准状况下1.12 L H2即n(H2)="0.05" mol,则电解NaCl溶液时消耗H2O电离出的H+的物质的量为0.1 mol,则产生的n(OH-)="0.1" mol,即 c(OH-)=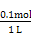 ="0.1" mol/L,所以pH=13。
="0.1" mol/L,所以pH=13。
本题难度:一般
4、选择题 a mol FeS与b mol FeO投入到V L、c mol・L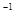 的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为
的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为
①(a+b)×63 g?②(a+b)×189 g
③(a+b) mol?④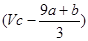 mol
mol
A.①④
B.②③
C.①③
D.②④
参考答案:D
本题解析:FeS和FeO在反应中共失去电子的物质的量是(a+8a+b)mol,所以被还原硝酸的物质的量是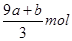 ,则没有被还原的硝酸的物质的量是
,则没有被还原的硝酸的物质的量是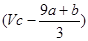 mol;根据铁原子守恒可知,没有被还原的硝酸是(3a+3b)mol,其质量是(a+b)×189 g,答案选D。
mol;根据铁原子守恒可知,没有被还原的硝酸是(3a+3b)mol,其质量是(a+b)×189 g,答案选D。
点评:该题是高考中的常见题型,属于中等难度的是,试题基础性强,侧重学生能力的考查。化学计算中的守恒法主要是指质量守恒定律、电子的得失守恒、原子守恒和电荷守恒等,需要学生在平时的训练中注意总结和积累。
本题难度:一般
5、选择题 将一定质量铜与100 mL一定浓度的硝酸反应,铜完全溶解时产生的NO和NO2混合气体在标准状况下的体积为11.2 L。待产生的气体全部释放后,向溶液加入140 mL 5 mol・L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的物质的量浓度是
A.5 mol/L
B.7 mol/L
C.10 mol/L
D.12 mol/L
参考答案:D
本题解析:在Cu与硝酸的反应中Cu失去电子变为Cu2+,硝酸得到电子变为NO和NO2混合气体,向反应后的溶液中加入OH-后,发生反应:Cu2++2OH-=Cu(OH)2↓.消耗的OH-的个数与硝酸铜中的硝酸根离子的个数相等。所以反应过程中消耗的硝酸的物质的量为n(HNO3)=n(气体)+n(NO3-)=" 11.2L÷22.4L/mol+" 0.14L×5 mol/L="0." 5mol+0.7mol=1.2mol.所以C(HNO3)=1.2mol÷0.1L=12mol/L.选项为D.
本题难度:一般