1��ѡ���� ��Fe2����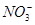 ��Fe3����
��Fe3����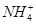 ��H����H2O�������ӣ�����ͬһ������ԭ��Ӧ�еķ�Ӧ��������������������ȷ����
��H����H2O�������ӣ�����ͬһ������ԭ��Ӧ�еķ�Ӧ��������������������ȷ����
A���������ͻ�ԭ�������ʵ���֮��Ϊ1��8
B���÷�Ӧ˵��Fe(NO3)2��Һ���˼����ữ
C��ÿ1 mol 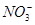 ����������Ӧ��ת��8 mol e��
����������Ӧ��ת��8 mol e��
D�����Ѹ÷�Ӧ���Ϊԭ��أ�����ӦΪFe2����e��=Fe3��
�ο��𰸣�C
�������������������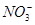 ����ǿ�����ԣ�Fe3��Ҳ���������ԣ���Ӧ��
����ǿ�����ԣ�Fe3��Ҳ���������ԣ���Ӧ��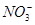 ��Fe2������ΪFe3�����÷�Ӧ�����ӷ���ʽΪ8Fe2����
��Fe2������ΪFe3�����÷�Ӧ�����ӷ���ʽΪ8Fe2����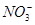 ��10H��=8Fe3����
��10H��=8Fe3����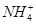 ��3H2O��B����ȷ���������뻹ԭ�������ʵ���֮��Ϊ1��8��A����ȷ��
��3H2O��B����ȷ���������뻹ԭ�������ʵ���֮��Ϊ1��8��A����ȷ��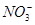 �е��Ļ��ϼ�Ϊ��5�ۣ�
�е��Ļ��ϼ�Ϊ��5�ۣ�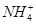 �е��Ļ��ϼ�Ϊ��3����1 mol
�е��Ļ��ϼ�Ϊ��3����1 mol 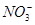 �����˻�ԭ��Ӧ��C�����ԭ��صĸ�������������Ӧ��D����ȷ��
�����˻�ԭ��Ӧ��C�����ԭ��صĸ�������������Ӧ��D����ȷ��
�����Ѷȣ�һ��
2��ѡ���� ��֪A2On2������B2����Ӧ��B2��������������ΪB���ʣ�A2On2������ԭ������ΪA3+����֪100mL c(A2On2��)=0.3mol/L����Һ��150mL c(B2��)="0." 6mol/L����Һǡ����ȫ��Ӧ����nֵΪ��?��
A��4
B��5
C��6
D��7
�ο��𰸣�D
������������ݻ��ϼ۹���A2On2-��A�Ļ��ϼ�Ϊ+��n-1����n��A2On2-��=0.1L��0.3mol/L=0.03mol��
n��B2-��=0.15L��0.6mol/L=0.09mol������ԭ��Ӧ���������ͻ�ԭ����ʧ������Ŀ��ȣ���0.03mol��2����n-1-3��=0.09mol����2-0��n=7��ѡD��
�����Ѷȣ�һ��
3��ѡ���� һ������CuS��Cu2S�Ļ����Ͷ��������HNO3�У��ռ�������VL����״��������Ӧ�����Һ�У�ͭԪ�ء���Ԫ�صĴ�����ʽ�ֱ�ΪCu2+��SO42-����������NaOHϡ��Һ��������ɫ���������ˣ�ϴ�ӣ����ճ������õ�CuO����12.0g������������ΪNO��NO2�Ļ����������Ϊ1�s1����VL����Ϊ
A��7.5L
B��9.5L
C��13.6L
D��16.8L
�ο��𰸣�B
����������������ȫ��CuS�������ʵ���Ϊ10=0.15mol������ת������0.15����6+2��=1.2mol�����������ȣ���NO xmol,NO2 xmol,3x+x1=1.2�������x=0.3���������V=0.6��22.4=13.44L���������ȫ��Cu2S,�����ʵ���Ϊ0.075mol,ת�Ƶ�����0.075��10=0.75mol�� ��NO xmol��NO2 xmol, 3x+x1=0.75�������x=0.1875���������0.375��22.4=8.4L�����ѡB��
�����Ѷȣ�һ��
4��ѡ���� �������ǿ��ʱ�ֽ�IJ����Ƕ�������.����.����.ˮ����÷�Ӧ���ϼ۱仯��δ�仯�ĵ�ԭ����֮��Ϊ
A��1��4
B��1��2
C��2��1
D��4��1
�ο��𰸣�B
���������3(NH4)2SO4=3SO2��+N2��+4NH3��+6H2O�����ϼ����ߵ�Nԭ���뻯�ϼ۲��仯��Nԭ�Ӹ�����Ϊ2��4��
�����������������д������ʽ�ٷ�����
�����Ѷȣ�һ��
5��ѡ���� п�ͺ�ϡ�������ַ�Ӧ��������п����������ʵ�����Ϊ1:2.5ʱ������������п��ˮ֮�������һ�����ʣ������ʿ�����
��NO2 ��.N2O ��.NO ��.NH4NO3
A���٢�
B���٢�
C���ڢ�
D���ۢ�