微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有一种氢氧燃料电池以30%KOH溶液为电解质溶液,工作时的电极反应如下:
2H2+4OH-- 4e-=4H2O? O2+2H2O+4e-=4OH-,下列说法中错误的是
A.电池工作时,电子由负极通过外电路流向正极
B.标准状况下,反应3.36L氢气,转移电子0.2mol
C.氢氧燃料电池能量利用率高于氢气直接燃烧的能量利用率
D.产物为无污染的水,属于环境友好电池
2、实验题 如下两个反应: A、NaOH+HCl=NaCl+H2O???? B、2FeCl3+Fe=3FeCl2
(1)根据两反应本质,分别判断能否用于设计原电池____________________________。其理由_________________________________________________________。
(2)如果可以,请画出实验装置图,注明电解质溶液名称和正负极材料,标出电子的流动方向,写出电极反应式。


________是正极,正极反应式:___________________;
________是负极,负极反应式:__________________。
3、填空题 (11分)电化学在工业生产中有广泛应用。
(1)右图所示装置中,两玻璃管及烧杯中是滴有酚酞的NaCl饱和溶液,
C(I)、C(II)为多孔石墨电极。
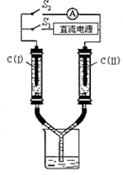
①电解NaCl饱和溶液的化学方程式为 。
②接通S1后,C(I)附近溶液变红,两玻璃管中有气体生成。则电极C(I)是 (填“阳”或“阴”)极;检验C(II)电极反应所得气体产物的方法和现象是 。
③一段时间后(玻璃管中液面未脱离电极),断开S1,则C(I)、C(II)两玻璃管内气体的体积V(I)、V(II)的关系是:V(I) V(II)(填“>”、 “=”或 “<”) 。断开S1接通S2,电流表的指针发生偏转,此时电极C(II)是 (填“正”或“负”)极;C(I)的电极反应是: 。
(2)若用此装置精炼粗铜,断开S2,接通S1,电解液选用CuSO4溶液,当电路中有0.04 mol电子通过时,阴极增重 g。
4、填空题 (13分)由方铅矿(PbS)制备Pb和PbO2的方法如下:
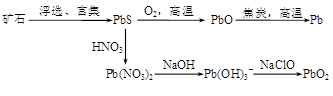
PbO与焦炭煅烧时可能会发生如下反应:
PbO(s)+C(s)=Pb(s)+CO(g)???? ΔH=+108.5 kJ・mol―1????? ①
PbO(s)+CO(g)=Pb(s)+CO2(g)?? ΔH=-64 kJ・mol―1??????? ②
(1)已知Pb与O2反应的热化学方程式为:2Pb(s)+O2(g)=2PbO(s)? ΔH=-438 kJ・mol―1
则C完全燃烧的热化学方程式为?????。
(2)能提高反应②中PbO转化率的措施有?????(填字母)。
a.升高温度??????? b.增大压强??????? c.加入焦炭??????? d.加入催化剂
(3)制备过程中会产生SO2、NO、CO等有毒气体,可将它们按一定比例混合在一定条件下反应得到S、N2和CO2。若SO2与NO的体积比为1∶2,该反应的化学方程式为???????。
(4)水溶液中铅的存在形态有多种,各形态的浓度分数α随溶液pH变化的关系如下图所示:
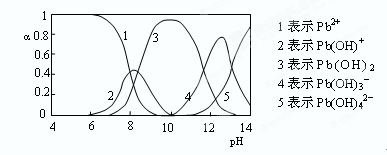
pH=6.5时,Pb2+水解的离子方程式为?????;加入NaClO制备PbO2之前需先用NaOH调节溶液pH至12.5,理由是?????。
5、选择题 现代生产、生活和国防中大量使用电池.下列有关电池的说法正确的是( )
A.碱性锌锰电池性能好于普通电池的原因是能反复使用
B.碱性锌锰电池的正极是MnO2,当电池中有6.5gZn反应时,将产生0.2molMnOOH
C.铅蓄电池放电时,负极的质量减少
D.使用碱性电解质的氢氧燃料电池,负极的电极反应是H2-2e-=2H+