��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� 1,2,3,4�����⻯���Ľṹ��ʽ����ͼ, ����ʽ��C10H12��������Ϊ��ɫҺ�壬�д̼�����ζ���е�207�棬������ˮ����һ���������ܼ�������Һ�巢����Ӧ��C10H12+ 4Br2�� C10H8Br4+ 4HBr���ɵ����廯��������Ϊ��̬��������ˮ�����������⻯����Һ�塢����ˮ�ʹ�����Ϊԭ�ϣ��Ʊ�����������������Һ��ʵ�鲽�����£�
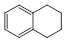

�ٰ�һ�������Ȱ����⻯����ˮ�����ʵ��������У��������������ۡ�
����������Һ�壬���Ͻ��裬ֱ����Ӧ��ȫ��
��ȡ�·�Ӧ�����������������⻯����ֱ����Һ��ɫ��ʧ�����ˣ�����Һ�����Һ©�������á�
�� ��Һ���õ��ġ�ˮ�㡱����������Һ��
�ش���������:
(1) ��ͼ��ʾ��װ��, �ʺϲ���ٺ͢ڵIJ�������????????????????????????��
(2) �����������жϡ���Ӧ��ȫ��_________________________________________��
(3) ������в����������⻯����Ŀ����??????????????????????????????????��??
(4) ������й��˺�õ��Ĺ���������____________??????????????_________��
(5) ��֪��ʵ�������£�������������Һ�������������������66%������廯��Ӧ������ȫ���������ˮ�����⻯����������Լ��1:____________(����С�����1λ)��
�ο��𰸣���? A ???��??��Һ����ɫ����ɫ(�Ⱥ�) ?????��
���������
���������(1) ���������IJ���Ҫ���֪���ʺϲ���ٺ͢ڵIJ�������Aѡ�
(2) ����Һ������Һ��������ɫ�����Բ�������жϡ���Ӧ��ȫ���ķ�������Һ����ɫ����ɫ(�Ⱥ�)��
(3)���ڷ�Ӧ���嵥���ǹ����ģ����Բ�����в����������⻯����Ŀ���dz�ȥ������嵥�ʡ�
��4�����ɵ����廯��������Ϊ��̬��������ˮ�����Բ�����й��˺�õ��Ĺ������������廯����
��5��������������Һ�������������������66%���������Һ��������100g������Һ��HBr��������66g��ˮ��������34g�����ݷ�Ӧ�Ļ�ѧ����ʽC10H12+ 4Br2 C10H8Br4+ 4HBr��֪������66gHBr��Ҫ���⻯����������
C10H8Br4+ 4HBr��֪������66gHBr��Ҫ���⻯���������� �����Բ������ˮ�����⻯����������Լ��1:0.8��
�����Բ������ˮ�����⻯����������Լ��1:0.8��
�����������ۺ���ǿ���ѶȽϴ�ѧ�����ۺ���������˸��ߵ�Ҫ������������ѧ���淶��ʵ����ơ��������������Ʊ���ʵ������⣬�ۺ���ǿ�����ۺ�ʵ������ϵ���ܣ��еĻ��ṩһЩ�µ���Ϣ�����Ҫ��ѧ���������桢ϸ�µ����⣬��ϵ��ѧ����֪ʶ�ͼ��ܣ�����֪ʶ����ȡ�Ǩ�ơ����飬ȫ��ϸ�µ�˼�����ܵó���ȷ�Ľ��ۡ�
�����Ѷȣ�һ��
2��ѡ���� ������Ũ��Ϊ5 mol��L ��NaOH��Һ���� 1 mol��L ��NaOH��Һ��Ӧȡ 5 mol��L��NaOH��Һ������ˮ�������ԼΪ��???��
A��1�� 4
B��1�� 5
C��2�� 1
D��2��3
�ο��𰸣�A
�������������Ҫ5 mol��L��NaOH��Һ������ˮ������ֱ���x��y��ϡ�����У����ʲ��䡣��5x����x��y����1�����x�Uy��1�U4����ѡA��
�����Ѷȣ���
3��ѡ���� ����ʵ���ܴ�ʵ��Ŀ����
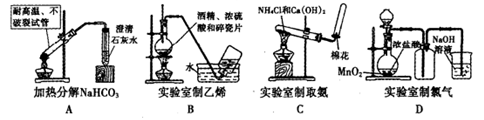
�ο��𰸣�A
���������
���������B����ȡ��ϩʱ���¶ȼƵ�ˮ����Ӧ��Һ�����£�����C���ռ�����ʱ��������Ӧ�嵽�Թܵײ�������D���ö���������Ũ���ᷴӦ��ȡ����ʱ��Ӧ�þƾ��Ƽ��ȣ�����
�����Ѷȣ�һ��
4��ѡ���� ����������Ʊ��ɲ�����ͼװ�õ���
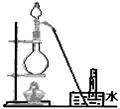
A?ͭ��Ũ���ᷴӦ��NO2
B?ͭ��ϡ���ᷴӦ��NO
C? Zn��1Ħ/�����ᷴӦ��H2
D?�Ȼ�����Ũ���ᷴӦ��HCl
�ο��𰸣�B
���������
���������NO2�ܺ�ˮ��Ӧ����NO�����ᣬ��������ˮ���ռ���A����ȷ��NO������ˮ�����ױ�������������NO2������Ӧ������ˮ���ռ���B��ȷ��п��ϡ���ᷴӦ�Ʊ���������Ҫ���ȣ�C����ȷ���Ȼ��⼫������ˮ����������ˮ���ռ���D����ȷ����ѡB��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ���Ի���֪ʶ���˽�������������ڹ���ѧ���Ļ��������ѧ����ʵ���������������Ĺؼ�����ȷ������Ʊ�ԭ����Ȼ����װ��ͼ������ü��ɣ��ѶȲ���
�����Ѷȣ�һ��
5��ʵ���� ��12�֣����������[(NH4)2SO4��FeSO4��6H2O]Ϊdz��ɫ���壬ʵ�����г��Է���мΪԭ�����Ʊ����䲽�����£�
����1?������м����̼������Һ����г����ۣ������Һ�壬��ˮϴ����м��
����2?����������м�м��������3mol��L��1 H2SO4��Һ����60������ʹ�䷴Ӧ�����ٲ������壬���ȹ��ˣ���FeSO4��Һ��
����3?������FeSO4��Һ�м��뱥��(NH4)2SO4��Һ��������һϵ�в�������õ���������茶��塣
��ش��������⣺
��1���ڲ���1�IJ����У����������в����õ�����__________����������ţ�
������̨? ��ȼ�ճ�? ����ƿ? �ܹ��ƿ? ���в�? ������? �߾ƾ���
��2���ڲ���2�г��ȹ��ˣ���ԭ����________________________________��
��3���ڲ���3�Ƶĵ���������茶��峣����Fe3+���ʡ�����Fe3+���Լ�������K4��Fe(CN)6��������³ʿ���������йص����ӷ���ʽ��_________________________ _____��
��4���Ƶõľ��徭�����˺�����ˮ�Ҵ�ϴ�Ӷ���������ˮ��������__________________������˵���㣩
��5����25��ʱ����ͬ���ʵ���Ũ�ȵ�(NH4)2CO3��(NH4)2SO4�������������������Һa��b��c����笠�����Ũ����С���������˳��Ϊ_______________����a��b��c�ش�
�ο��𰸣���1���ڢܢݣ���2����ֹ��Һ��ȴʱ��������������������ʧ��<
�����������1������I�dz�ȥ���ۣ�������Ҫ���ȣ����Ԣڢܢ��Dz���Ҫ�ġ�
��2�����������������ܽ�����¶ȵĽ��Ͷ����ͣ����Գ��ȹ��˵�Ŀ���Ƿ�ֹ��Һ��ȴʱ��������������������ʧ��
��3�����ݷ�Ӧ�����������Եó�����ʽΪK+��Fe3+��[Fe(CN)6]4��=KFe[Fe(CN)6]����
��4��������������茶������Ҵ��е��ܽ��С���ɼ�С������ϴ��ʱӦ�ܽ����ʧ����ξƾ��ӷ������ḽ���ھ�����档
��5��NH4��ˮ�������ԣ�CO32��ˮ���Լ��ԣ�������ٽ���Fe2��ˮ�������ԣ���NH4��ˮ������ƣ�����笠�����Ũ����С���������˳��Ϊa<b<c��
�����Ѷȣ�һ��