��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ҹ���ѧ�Һ�°�ĸ����Ĵ����������գ��������̿ɼ�Ҫ��ʾ���£�
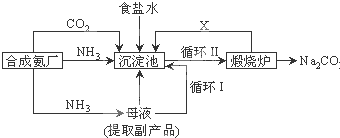
��1��������������ķ�����______������Ʒ��һ����;Ϊ______��
��2���������з����Ļ�ѧ��Ӧ����ʽ��______��
��3��д������������X���ʵķ���ʽ______��
��4��ʹԭ���Ȼ��Ƶ������ʴ�70%��ߵ�90%���ϣ���Ҫ�������______�������������еı�ţ���ѭ�����ӳ�������ȡ�������IJ�����______��
��5��Ϊ�����Ʒ̼�������Ƿ����Ȼ��ƣ���ȡ������������ˮ���ٵμ�______��
�ο��𰸣���1��Ŀǰ��ҵ�Ƽ���ж�������������Ƽ�����з�������
���������
�����Ѷȣ�һ��
2������� ��ҵ��������Ĺ�������ʾ��ͼ����

���������գ�
��1������ˮ���������A��B�����ʣ�������A��Դ��ʯ��Ҥ������д��A��B�Ļ�ѧʽ��
A_________B_________
��2��ʵ�����ᴿ���ε�ʵ���������Ϊ��ȡ����_________��������_________��_________����ȴ�ᾧ��_________����ɡ�
��3����ҵ��������������У�̼�ữʱ������������__________________��̼�ữʱû������̼���ƾ��壬��ԭ����__________________��
��4��̼�ữ����ˣ���ҺD����Ҫ�ijɷ���_________����д��ѧʽ����������һ�ɷֵ������ӵľ��巽���ǣ�__________________��
��5����������а���ѭ��ʹ�õģ�Ϊ�ˣ���ҺD����ʯ��ˮ����������ʯ��ˮ���������ķ�Ӧ�����ӷ���ʽΪ��__________________��ҺD��ʯ��ˮǰ��Ҫ���ȣ�ԭ����__________________��
��6����Ʒ�����к���̼�����ơ�����ü��ȷֽ�ķ����ⶨ������̼�����Ƶ�����������������̼�����Ƶ����������ɱ�ʾΪ��__________________��ע����ı���ʽ�����õ��йط��ŵĺ��壩
�ο��𰸣���1��Ca(OH)2��CaO��Na2CO3
��2���ܽ�
���������
�����Ѷȣ�����
3������� ����ѡһ��ѧ�뼼����
��ˮ���ۺ����ã����������������������Ҫ�����塣
��1����ˮ�����غ�ȱˮ������ȡ��ˮ�ķ���֮һ���оٳ���ˮ���������ַ���_____________��________________��
��2���ȼҵ���ӽ���Ĥ�������У������ӽ���Ĥ������Ϊ_____________���������Ʋ�����____________�����������������������
��3���Ȼ���Ϊ��ҵ�ƴ������Ҫԭ�ϣ��ƼӦ�����з�������NaHCO3��ԭ����______________�������Ƽ������ά�Ƽ��ȳ����ʳ�������ʡ����Ȼ������ɵ��������______________?��_______________?�Ӷ��ۺ�����ԭ�ϡ����ͳɱ������ٻ�����Ⱦ��
�ο��𰸣���1������ ��?��������
��2��Na+������
���������
�����Ѷȣ�һ��
4������� ij��ѧС��ģ�⡰�����Ƽ������NaCl��NH3��CO2��ˮ��Ϊԭ���Լ�ͼ1��ʾװ����ȡNaHCO3����Ӧ�Ļ�ѧ����ʽΪ��
NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl��Ȼ���ٽ�NaHCO3�Ƴ�Na2CO3��
��1��װ���ҵ�������______��Ϊ��ֹ��Ⱦ������β���к��е�______��Ҫ�������մ�����
��2����װ�ñ��в�����NaHCO3��ȡNa2CO3ʱ����Ҫ���е�ʵ�������______��ϴ�ӡ����գ�
��3�����ڣ�2�������յ�ʱ��϶̣�NaHCO3���ֽⲻ��ȫ����С���һ�ݼ�����t1min��NaHCO3��Ʒ����ɽ������о���ȡ������t1min��NaHCO3��Ʒ29.6g��ȫ����ˮ�Ƴ���Һ��Ȼ�������Һ�л����صμ�ϡ���ᣬ�����Ͻ��裮��������ļ��룬��Һ���й����ӵ����ʵ����ı仯��ͼ2��ʾ��������c��Ӧ����Һ�е�������______�������ӷ��ţ�������Ʒ��NaHCO3��Na2CO3�����ʵ���֮����______��
��4����ȡ10.5gNaHCO3���壬������t1min��ʣ����������Ϊ7.4g������Ѵ�ʣ�����ȫ�����뵽200mL1mol/L�������У����ַ�Ӧ����Һ��H+�����ʵ���Ũ��Ϊ______������Һ����仯���Բ��ƣ���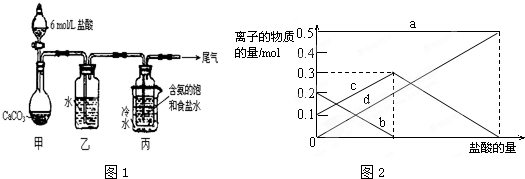
�ο��𰸣���1��װ�ü����Ʊ�������̼����ķ�Ӧװ�ã����ɵĶ�����̼����
���������
�����Ѷȣ���
5������� ijУѧ����ʵ���������������װ�ã�ģ���°��Ƽ�����̼�����ƾ��壬��Ӧԭ���������»�ѧ����ʽ��ʾ��NH3+CO2+NaCl+H2O�TNH4Cl+NaHCO3�������ݴ�ԭ�����ٽ�̼�����ƾ�����ȷֽ���Ƶ�̼���ƾ��壬����Bװ���е��Թ��������а����Ȼ��Ƶ���Һ���Ҷ��߾��Ѵﵽ���ͣ�
��1��Aװ�õ������ǣ�______��Cװ����ϡ���������Ϊ��______��ʹ�����θ���ܵ�Ŀ���ǣ�______��
��2���±������г�������������ڲ�ͬ�¶��µ��ܽ�����ݣ�g/100gˮ��
| 0�� | 10�� | 20�� | 30�� | 40�� | 50��
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
NaHCO3
6.9
8.1
9.6
11.1
12.7
14.5
NH4Cl
29.4
33.3
37.2
41.4
45.8
50.4
���ձ������ݣ������Bװ����ʹ�ñ�ˮ����Ϊ______��
��3����Уѧ���ڼ�������װ�������Ժ����ʵ�飬���û�еõ�̼�����ƾ��壬ָ����ʦָ��Ӧ��______װ��֮�䣨��д��ĸ������һ��ʢ��______��ϴ��װ�ã���������______��
��4������Уѧ������ʵ��ʱ�����ñ���ʳ��ˮ�к�NaCl������Ϊ5.85g��ʵ���õ������NaHCO3���������Ϊ5.04g����NaHCO3�IJ���Ϊ______��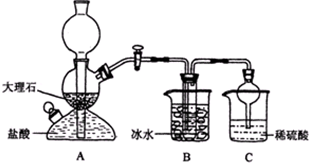
�ο��𰸣���1������װ��ͼ������AΪ���շ�������������ȡ�����Һ�岻��
���������
�����Ѷȣ�һ��
|