微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
实验编号
| c(HA)/ mol・L-1
| c(NaOH)/ mol・L-1
| 反应后溶液pH
|
甲
| 0.1
| 0.1
| pH=9
|
乙
| c1
| 0.2
| pH=7
下列判断不正确的是
A.c1一定大于0.2 mol・L-1
B.HA的电离方程式是HA
参考答案:
本题解析:
本题难度:一般
2、计算题 在25℃下,将a mol・L-1的氨水与0.01mol・L-1的盐酸等体积混合后,溶液中c(NH4+)=c(Cl-)。试用含a的代数式计算NH3・H2O的电离常数Kb。
参考答案: 本题解析:略 本题解析:略
本题难度:简单
3、选择题 室温时,将0.10 mol/L的NaOH溶液滴入20.0 mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积变化曲线如图。下列有关说法不正确的是
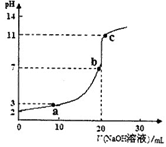
A.该一元酸溶液浓度为0.10mol/L
B.a、b、c点的水溶液导电性依次增强
C.室温时,HA的电离常数Ka l×10-5 l×10-5
D.a点和c点所示溶液中H2O的电离程度相同
参考答案:C
本题解析:
试题分析:A.NaOH、HA是一元碱、一元酸,当二者恰好完全反应时二者的物质的量相等,体积也相等,说明它们的浓度相等,该一元酸溶液浓度也相等,为0.10mol/L,正确;B.向弱酸溶液中加入强碱NaOH,发生中和反应产生盐,自由移动的离子浓度增大,溶液的导电性增强;当加入至酸完全反应时,自由移动离子进一步增多,离子浓度增大,溶液的导电性增强;后在加入NaOH,就相当与向盐NaA溶液中加入NaOH溶液。溶液中自由移动离子浓度增大,所以溶液的导电性比b点还强。故a、b、c点的水溶液导电性依次增强,正确;C.在未滴加NaOH溶液时,溶液的pH="2," c(H+)=10-2mol/L,NaOH是强碱,完全电离,当NaOH溶液滴入20ml时,恰好与酸HA完全反应,此时溶液的pH>7,说明得到的是强碱强弱酸盐,因此HA是弱酸,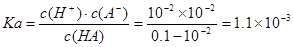 ,错误;D.a点时酸过量,c(H+)=10-3mol/L, c点时碱过量,c(H+)=10-11mol/L,c(OH-)=Kw÷c(H+)=10-14÷10-11=10-3mol/L,所以二者对水的电离平衡的抑制作用相同,因此这两点所示溶液中H2O的电离程度相同,正确。 ,错误;D.a点时酸过量,c(H+)=10-3mol/L, c点时碱过量,c(H+)=10-11mol/L,c(OH-)=Kw÷c(H+)=10-14÷10-11=10-3mol/L,所以二者对水的电离平衡的抑制作用相同,因此这两点所示溶液中H2O的电离程度相同,正确。
考点:考查电解质强弱的判断、物质浓度的计算及对水电离平衡的移动的影响的知识。
本题难度:困难
4、选择题 中和c(H+)相同、体积相同的H2SO4、HCl和CH3COOH溶液,耗用同一浓度的NaOH溶液,体积分别为
V1、V2和V3,则V1、V2和V3的关系正确的是[???? ]
A.V1>V2=V3
B.V3>V2=V1
C.V1>V2>V3
D.V1=V2=V3
参考答案:B
本题解析:
本题难度:一般
5、选择题 pH="2" 的两弱酸HA.HB加水稀释后,溶液 pH随加水量的变化曲线如图所示。则下列叙述正确的是:(?)
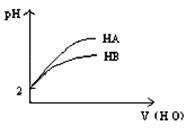
A.电离平衡常数HA > HB
B.等体积等pH的HA 和HB与等浓度的NaOH反应,HA消耗的NaOH多
C.等体积等pH的HA和HB 与等质量的Zn反应,HA反应速率大
D.若有等浓度的NaA.NaB,则碱性NaA>NaB
参考答案:A
本题解析:
试题分析:依据图示可知,两种酸都是弱酸,稀释过程中HA的PH变化比HB大,说明酸性HA大于HB;A.由于酸性HA>HB,故电离平衡常数HA>HB,A正确;B.酸性HA>HB,等PH时,HA的浓度一定小于HB的,由等体积,HA的物质的量一定小于HB的物质的量,HB消耗的氢氧化钠多,B错误;C.等体积等pH的HA和HB 与等质量的Zn反应,酸性HA>HB,浓度HA<HB,反应前溶液中氢离子浓度相等,反应中氢离子浓度HB的变化小,故与锌反应,开始时速率相等,之后HB的反应速率大,C错误;D.对应的酸的酸
本题难度:一般
|