��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��16�֣���ҵ�Ͽ����ں����ܱ������в������з�Ӧ�Ʊ��״���
CO��g����2H2��g�� CH3OH��g��
CH3OH��g��
��1���������������Ϊ�жϷ�Ӧ�ﵽƽ��״̬�����ݵ��ǣ�����ţ�????????????????��
A������CH3OH ������������H2������֮��Ϊ1�U2
B����������ƽ����Է����������ֲ���
C�����������ܶȱ��ֲ���
D����ϵ�ڵ�ѹǿ���ֲ���
��2���±���������Ϊ�÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����
�¶�/��
| 250
| 300
| 350
|
K
| 2.041
| 0.270
| 0.012
?
�ٷ�Ӧ��ƽ�ⳣ������ʽΪK=??????????�����ϱ������жϣ��÷�Ӧ�ġ�H????0����������������������������¶ȣ�����Ӧ����???????�����������С�����䡱����
��ij�¶��£���2molCO��6molH2����һ���ݻ�Ϊ2L���ܱ������У��ﵽƽ��ʱc(H2)=1.4mol/L����CO��ת����Ϊ????????����ʱ���¶�Ϊ?????????��
��3�������CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��????????????????��������ţ�
A������
B���������Ч�Ĵ���
C�����������³���CO
D�����������³���H��
E�����������³��뺤��
F����ʱ����CH3OH
��4��һ�������£�CO��H2�ڴ�������������1molCH3OH�������仯Ϊ90.8kJ�����¶��£��������ݻ���ͬ���ܱ������У�����ͬ��ʽͶ�ϣ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
����
| ��
| ��
| ��
| Ͷ�Ϸ�ʽ
| 1molCO��2molH2
| 1molCH3OH
| 2molCH3OH
| ƽ������
| C(CH3OH)/(mol/L)
| c1
| c2
| c3
| ��ϵѹǿ(Pa)
| p1
| p2
| p3
| ��Ӧ�������仯
| akJ
| bkJ
| ckJ
| ԭ��ת����
| ��1
| ��2
| ��3
?
���з�����ȷ����?????????????��������ţ�
A��2c1��c3????????B��2 p1��p3?????C��|a|��|b|��90.8???? D����1����3��1
2��ѡ���� ij�¶��£� ��ƽ�ⳣ��K=9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�����±� ��ʾ�� ��ƽ�ⳣ��K=9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�����±� ��ʾ��
| 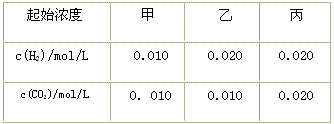 ? ?
�����жϲ���ȷ���� [???? ]
A��ƽ��ʱ������CO2��ת���ʴ���60%
B��ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C��ƽ��ʱ������c(CO2)�Ǽ��е�2������0.012 mol/L
D����Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
3��ѡ���� ��25��ʱ���ܱ�������X��Y��Z��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±���
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772