微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列电池工作时能量转化形式与其它三个不同的是

参考答案:B
本题解析:
试题分析:A、原电池把化学能转化为电能;B、把太阳能转化为电能;C、化学能转化为电能;D、化学能转化为电能,因此答案选B。
考点:考查能量转化的判断
本题难度:一般
2、填空题 (14分)⑴甲同学根据漂白液的制备原理和电解原理制作了一种家用环保型消毒液发生器(如图所示),用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源中b为____极,阳极电极反应式为: __________________________;生成漂白液的离子方程式为___________________________________________。
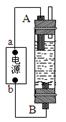
⑵乙同学受此启发,借用此装置制取Fe(OH)2,电解质溶液为硫酸钠溶液,B电极材料为石墨,A电极材料为_________,电极反应式为:A极____________________。通电后,溶液中产生白色沉淀,且较长时间不变色。则看到明显现象后,将电极反接电源,通电后,除了能观察到两极有气泡外还能观察到的明显现象是_____________________________________________________,发生此现象的化学方程式是____________________________________________________。
参考答案:(1)正??? 2Cl--2e-=Cl2↑????? Cl2
本题解析:(1)根据装置图可知,A电极生成氢气,被收集,所以A电极是阴极,则a是电源的负极,b是电源的正极,B是电解池的阳极,溶液中的氯离子放电,电极反应式是2Cl--2e-=Cl2↑。由于阴极还产生氢氧化钠,所以生成的漂白液的方程式是Cl2+2OH-=Cl-+ClO-+H2O。
(2)要生成氢氧化亚铁,则A电极材料一定是铁,电极反应式是Fe-2e-=Fe2+。电极反接后,阳极是溶液中的OH-放电,生成氧气。由于氢氧化亚铁极易被氧化,所以现象是白色絮状沉淀迅速变成灰绿色,最终变成红褐色,方程式是4Fe(OH)
本题难度:一般
3、简答题 化学电池在通讯、交通及日常生活中有着广泛的应用.
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为
Cd+2NiO(OH)+2H2O
放电
充电
2Ni(OH)2+Cd(OH)2.
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是______.
①放电时NiO(OH)作负极
②充电时Cd(OH)2发生还原反应
③充电时化学能转变为电能
④放电时化学能转变为电能
(2)废弃的镍镉电池已成为严重的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值.在酸性土壤中这种污染尤为严重,这是因为______.

参考答案:(1)放电时Cd作负极,发生氧化反应生成Cd(OH)2;而充
本题解析:
本题难度:简单
4、填空题 (12分)近年来北京市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
(1)汽车内燃机工作时引起反应:N2(g)+O2(g)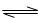 2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向容积为2 L的密闭容器中充入10molN2与5molO2,达到平衡后NO的物质的量为2mol,则T℃时该反应的平衡常数K=??????????。(计算结果保留小数点后两位数字)
2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向容积为2 L的密闭容器中充入10molN2与5molO2,达到平衡后NO的物质的量为2mol,则T℃时该反应的平衡常数K=??????????。(计算结果保留小数点后两位数字)
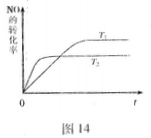
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如图14所示。(已知: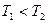 )
)
①反应2NO(g)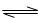 N2(g)+O2(g)为(填“吸热”或“放热)??????????????反应。
N2(g)+O2(g)为(填“吸热”或“放热)??????????????反应。
②一定温度下,能够说明反应2NO(g)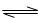 N2(g)+O2(g)已达到平衡的是(填序号)?????????。
N2(g)+O2(g)已达到平衡的是(填序号)?????????。
a.容器内的压强不发生变化
b.NO、N2、O2的浓度保持不变
c.NO分解的速率和NO生成的速率相等
d.单位时间内分解4mol NO,同时生成2 mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)?△H1=-574kJ・mol-1
CH4(g)+4NO(g)=2N2(g)=CO2(g)+2H2O(g)??△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)??△H3=-867kJ・mol-1
△H2=??????????????.
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NO2)转化为无毒气体,该反应的化学方程式为?????。
参考答案:
(1)0.11(1/9给分)????? ………………
本题解析:略
本题难度:一般
5、选择题 以下现象与电化腐蚀无关的是
A.黄铜(铜锌)制作的铜锣不易产生铜绿
B.生铁比纯铁易生锈
C.铁质器件附有铜质配件,在接触处易生铁锈
D.银质奖牌久置后表面变暗
参考答案:D
本题解析:
试题分析:A.黄铜(铜锌合金)制作的铜锣中,金属锌为负极,金属铜做正极,Cu被保护,不易腐蚀,和电化学腐蚀有关,错误;B.生铁中金属铁、碳、潮湿的空气能构成原电池,金属铁为负极,易被腐蚀而生锈,和电化学腐蚀有关,错误;C.铁质器件附有铜质配件,在接触处形成原电池装置,其中金属铁为负极,易生铁锈,和电化学腐蚀有关,错误;D.银质奖牌长期放置后在其奖牌的表面变暗是由于金属银和空气中的氧气发生反应生成氧化银的结果,属于化学腐蚀,与电化学腐蚀无关,选D。
考点:金属的电化学腐蚀与防护。
本题难度:一般