微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
A.稀释前,c(A)=10?c(B)
B.稀释前,A溶液中由水电离出的OH-的浓度大于10-7?mol/L
C.在M点,A、B两种碱溶液中阳离子的物质的量浓度相等
D.用醋酸中和A溶液至恰好完全反应时,溶液的pH为7
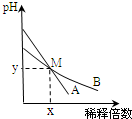
参考答案:A、稀释前,c(AOH)=0.1mol/L,c(BOH)>0
本题解析:
本题难度:一般
2、填空题 某温度下,Kw=1×10-13。该温度下,将pH= a,体积为Vx的H2SO4与pH=b,体积为Vy的NaOH混合。
(1)若混合后溶液呈中性。①如果Vx =Vy,则a+b = ,②若a+b = 11,则Vx:Vy= 。
(2)若混合后溶液的pH=3,且a=2、b=10,则Vx:Vy= 。
(3)将pH= a,体积为Vx的CH3COOH和H2SO4分别加m mL和n mL水稀释,稀释后的pH均为a+2,则m n。(填“>”、“<”或“=”)
参考答案:(1)① 13
本题解析:
试题解析:(1)由题意知KW=1×10-13,故中性溶液的pH=6.5,若混合后溶液呈中性,即酸碱恰好反应,所以10-a× Vx=10b-13×Vy,则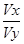 =
=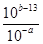 =10a+b-13,①如果Vx =Vy,则a+b =13,②若a+b = 11,则Vx:Vy=1:100;(2)若混合后溶液的pH=3,则溶液显酸性,混合后溶液的PH=
=10a+b-13,①如果Vx =Vy,则a+b =13,②若a+b = 11,则Vx:Vy=1:100;(2)若混合后溶液的pH=3,则溶液显酸性,混合后溶液的PH=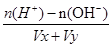 =
=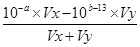 =
= =10-3,解得Vx:Vy=2:9;(3)CH3COOH为弱酸,稀释过程中又电离出氢离子,醋酸在稀释过程中PH变化小,H2SO4是强酸稀释过程中PH变化大,分别加m mL和n mL水稀释,且稀释后的pH均为a+2,则醋酸稀释的倍数大,故m大于n。
=10-3,解得Vx:Vy=2:9;(3)CH3COOH为弱酸,稀释过程中又电离出氢离子,醋酸在稀释过程中PH变化小,H2SO4是强酸稀释过程中PH变化大,分别加m mL和n mL水稀释,且稀释后的pH均为a+2,则醋酸稀释的倍数大,故m大于n。
考点:酸碱混合的PH计算
本题难度:一般
3、选择题 相同温度、相同浓度下的六种电解质溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别为( )
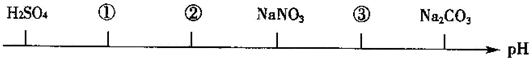
A.CH3COOH;HCl;CH3COONa
B.HCl;CH3COOH;CH3COONa
C.NH4Cl;CH3COOH;NaOH
D.NH4Cl;HCl;NaHCO3
参考答案:硫酸是强酸,其溶液呈酸性,硝酸钠是强酸强碱盐,其溶液呈中性,
本题解析:
本题难度:一般
4、选择题 已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中
c(H+)/c(CH3COOH)值增大,可以采取的措施是
[???? ]
A.加少量烧碱溶液
B.升高温度
C.加少量冰醋酸
D.加水
参考答案:BD
本题解析:
本题难度:一般
5、填空题 (8分)取0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因是??????????????????????????????(用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+)???????0.1 mol/L NaOH溶液中由水电离出的c(H+) (填“>”、“<”或“=”)。
(3)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH???????7(填“>”、“<”或“=”)。
(4)有相同温度下相同浓度的四种盐溶液:
A.NH4HCO3;
B.NH4A;
C.(NH4)2SO4;
D.NH4Cl,按pH由大到小的顺序排列(填序号)。
参考答案:(共8分,每空2分)(1)A-+H2O 本题解析:
本题解析:
试题分析:(1)等物质的量的一元酸和一元碱恰好反应生成盐和水,生成的盐溶液呈碱性说明该酸是弱酸,生成的盐能水解导致溶液中氢氧根离子浓度大于氢离子浓度,溶液的pH值大于7,水解方程式为:A-+H2O HA+OH-;
HA+OH-;
(2)该盐含有弱根离子能促进水电离,氢氧化钠是强碱能抑制水电离,所以混合溶液中由水电离
本题难度:一般