微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在含1mol KAl(SO4)2的溶液中逐滴加入2mol Ba(OH)2溶液,下列有关说法中正确的是
A.先生成沉淀,后沉淀全部溶解
B.当溶液中Al3+全部沉淀出来时,沉淀的总物质的量最大
C.最后得到的沉淀是BaSO4
D.最后的沉淀为2mol BaSO4、1mol Al(OH)?3
参考答案:AC
本题解析:KAl(SO4)2的电离方程式为:KAl(SO4)2=K++AL3++2SO42-;1mol KAl(SO4)2中含K+1mol,AL3+1mol,SO42-2mol,当逐滴加入Ba(OH)2溶液时,立即有AL(OH)3沉淀和BaSO4沉淀生成,当加入的Ba(OH)2的物质的量达到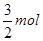 时,AL3+全部生成AL(OH
时,AL3+全部生成AL(OH
本题难度:一般
2、选择题 下列叙述正确的是( )
A.将二氧化硫气体通入浅黄色的溴水中使其颜色褪去,说明二氧化硫具有漂白性
B.SiO2为碳族元素的非金属氧化物为酸性氧化物,故不能与任何酸发生化学反应
C.用砂纸打磨过的铝箔放在酒精灯焰上不燃烧,说明铝不易与O2反应
D.向装有NaHCO3溶液的两支试管中各滴入CaCl2和MgCl2的饱和溶液,后者有沉淀呈现
参考答案:A、将二氧化硫气体通入浅黄色的溴水中使其颜色褪去,是因为发生
本题解析:
本题难度:一般
3、简答题 (14 分)铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlC13(g)+3C(s) ="3AlCl(g)+3CO(g)" ??△H="a" kJ・mol-1
3AlCl(g)=2Al(l)+AlC13(g)?△H="b" kJ・mol-1
①反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=????????kJ・mol-1(用含a、b 的代数式表示)。
②Al4C3是反应过程中的中间产物。Al4C3与盐酸反应(产物之一是含氢量最高的烃) 的化学方程式为????????????????????????????????????????????。
(2)镁铝合金(Mg17Al12 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg17Al122+17H2=17MgH2+12Al。得到的混合物Y(17MgH2 +12Al)在一定条件下可释放出氢气。???
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是???????????????????????。
②在6. 0 mol・L-1 HCl 溶液中,混合物Y 能完全释放出H2。1 mol Mg17 Al12完全吸氢后得到的混合物Y 与上述盐酸完全反应,释放出H2的物质的量为????????????。
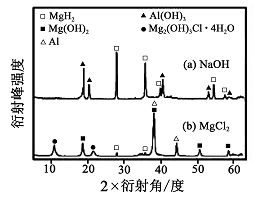
③在0. 5 mol・L-1 NaOH 和1. 0 mol・L-1 MgCl2溶液中,?????????????????图8
混合物Y 均只能部分放出氢气,反应后残留固体物质的X-射线衍射谱图如图所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。在上述NaOH 溶液中,混合物Y 中产生氢气的主要物质是???????????????????????(填化学式)。
(3)铝电池性能优越,Al-AgO 电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为 ?????????????????????????????????。

参考答案:(1)①a+b????②Al4C3+12HCl=4AlCl3
本题解析:(1)根据盖斯定律,将题中所给两方程式相加得所求反应,对应的△H=(a+b)kJ・mol-1。含氢量最高的烃为CH4,根据碳原子守恒,3个碳需要结合12个H原子形成3个CH4。再由铝原子守恒,4个铝需要结合12个Cl形成4个AlCl3,所以Al4C3与HCl之间为1:12参加反应。(2)①镁、铝都是活泼的金属单质,容易被空气中的氧气氧化,通入氩气作保护气,以防止二者被氧化。②1mol Mg17Al12完全吸氢 17mol,在盐酸中会全部释放出来。镁铝合金中的镁和铝都能与盐酸反应生成H2,物质的量分别为17
本题难度:一般
4、选择题 某同学通过系列实验探究Mg及其化合物的性质, 操作正确且能达到目的的是
操作正确且能达到目的的是
A.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成
B.将水加入浓硫酸中得到稀硫酸,置镁片于其中探究讨Mg的活泼性
C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
D.将Mg(OH)2沉淀转入表面皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体
参考答案:A
本题解析:
试题分析:A符合复分解反应发生的条件。正确。B浓硫酸稀释的原则是要注酸入水。错误。C.将Mg(OH)2浊液通过玻璃棒引流到已装好滤纸的漏斗中过滤,洗涤并收集沉淀。错误。D.Mg(OH)2沉淀加足量稀盐酸溶解,然后在氯化氢的氛围中加热蒸干溶液得无水MgCl2固体,错误。
本题难度:一般
5、填空题 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则溶液中MgCl2与
Al2(SO4)3的物质的量浓度之比为 ___________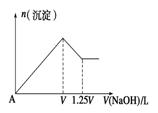
参考答案:1:1(3分)
本题解析:略
本题难度:简单